
| A£® | Éś³É22.4LN2£Ø±ź×¼×“æö£© | B£® | ÓŠ0.25molKNO3±»Ńõ»Æ | ||
| C£® | ×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ0.5mol | D£® | ±»Ńõ»ÆµÄNŌ×ÓµÄĪļÖŹµÄĮæĪŖ3mol |
·ÖĪö 10NaN3+2KNO3ØTK2O+5Na2O+16N2”üÖŠ£¬Ö»ÓŠNŌŖĖŲ»ÆŗĻ¼Ū·¢Éś±ä»Æ£¬NŌŖĖŲµÄ»ÆŗĻ¼Ū·Ö±šÓÉøŗ¼ŪÉżøßĪŖ0”¢ÓÉ+5¼Ū½µµĶĪŖ0£¬øł¾Ż·“Ó¦·½³ĢŹ½æÉÖŖ£¬Ćæµ±Éś³É16molN2£¬ŌņŃõ»Æ²śĪļ±Č»¹Ō²śĪļ¶ą14mol£¬×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ10mol£¬±»Ńõ»ÆµÄNŌ×ÓµÄĪļÖŹµÄĮæĪŖ30mol£¬ÓŠ2molKNO3±»»¹Ō£¬ČōŃõ»Æ²śĪļ±Č»¹Ō²śĪļ¶ą1.4mol£¬ŌņÉś³É1.6molN2£¬×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ1mol£¬±»Ńõ»ÆµÄNŌ×ÓµÄĪļÖŹµÄĮæĪŖ3mol£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗ10NaN3+2KNO3ØTK2O+5Na2O+16N2”üÖŠ£¬Ö»ÓŠNŌŖĖŲ»ÆŗĻ¼Ū·¢Éś±ä»Æ£¬NŌŖĖŲµÄ»ÆŗĻ¼Ū·Ö±šÓÉøŗ¼ŪÉżøßĪŖ0”¢ÓÉ+5¼Ū½µµĶĪŖ0£¬øł¾Ż·“Ó¦·½³ĢŹ½æÉÖŖ£¬Ćæµ±Éś³É16molN2£¬ŌņŃõ»Æ²śĪļ±Č»¹Ō²śĪļ¶ą14mol£¬×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ10mol£¬±»Ńõ»ÆµÄNŌ×ÓµÄĪļÖŹµÄĮæĪŖ30mol£¬ÓŠ2molKNO3±»»¹Ō£¬ČōŃõ»Æ²śĪļ±Č»¹Ō²śĪļ¶ą1.4mol£¬ŌņÉś³É1.6molN2£¬×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ1mol£¬±»Ńõ»ÆµÄNŌ×ÓµÄĪļÖŹµÄĮæĪŖ3mol£¬
A£®Éś³É1.6molN2£¬Ģå»żĪŖ1.6mol”Į22.4L/mol=35.64L£¬¹ŹA“ķĪó£»
B£®ÓÉŅŌÉĻ·ÖĪöæÉÖŖÓŠ0.2molKNO3±»»¹Ō£¬¹ŹB“ķĪó£»
C£®×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ1mol£¬¹ŹC“ķĪó£»
D£®²Ī¼Ó·“Ó¦µÄNaN3ĪļÖŹµÄĮæĪŖ1mol£¬Ōņ±»Ńõ»ÆµÄNŌ×ÓµÄĪļÖŹµÄĮæĪŖ3mol£¬¹ŹDÕżČ·£®
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĮĖŃõ»Æ»¹Ō·“Ó¦£¬øł¾ŻŌŖĖŲ»ÆŗĻ¼Ū±ä»Æ½įŗĻø÷øöĪļĄķĮæÖ®¼äµÄ¹ŲĻµŹ½·ÖĪö½ā“š£¬×¢ŅāµŖ»ÆÄĘÖŠNŌŖĖŲ»ÆŗĻ¼Ū£¬øĆ·“Ó¦µÄŃõ»Æ²śĪļŗĶ»¹Ō²śĪļ¶¼ŹĒµŖĘų£¬ÖŖµĄŃõ»Æ²śĪļŗĶ»¹Ō²śĪļµÄĪļÖŹµÄĮæÖ®±Č£¬ĪŖŅדķµć£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ÓĆĒ¦Šīµē³Ųµē½ā¼×”¢ŅŅµē½ā³ŲÖŠµÄČÜŅŗ£®ŅŃÖŖĒ¦Šīµē³ŲµÄ×Ü·“Ó¦ĪŖ£ŗ
ÓĆĒ¦Šīµē³Ųµē½ā¼×”¢ŅŅµē½ā³ŲÖŠµÄČÜŅŗ£®ŅŃÖŖĒ¦Šīµē³ŲµÄ×Ü·“Ó¦ĪŖ£ŗ| A£® | d¼«ĪŖŅõ¼« | |
| B£® | ·ÅµēŹ±Ē¦Šīµē³Ųøŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗPbO2£Øs£©+4H+£Øaq£©+SO42-£Øaq£©+4e-ØTPbSO4 £Øs£©+2H2O £Øl£© | |
| C£® | ČōĄūÓĆ¼×³Ų¾«Į¶Ķ£¬b¼«Ó¦ĪŖ“ÖĶ | |
| D£® | ČōĖÄøöµē¼«²ÄĮĻ¾łĪŖŹÆÄ«£¬µ±Īö³ö6.4 g CuŹ±£¬Į½³ŲÖŠ¹²²śÉśĘųĢå3.36 L£Ø±ź×¼×“æöĻĀ£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ö»ÓŠ¢Ł¢Ś | B£® | Ö»ÓŠ¢Ü¢Ż | C£® | Ö»ÓŠ¢Ł¢Ś¢Ż | D£® | Ö»ÓŠ¢Ł¢Ś¢Ū¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | H2 | B£® | O2 | C£® | HBr | D£® | Br2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŗĻ³É¼×“¼£ŗCO+2H2$”ś_{¼ÓČČ¼ÓŃ¹}^{“߻ƼĮ}$CH3OH | |
| B£® | ŗĻ³ÉŅŅČ©£ŗ2CH2=CH2+O2$”ś_{¼ÓČČ¼ÓŃ¹}^{“߻ƼĮ}$2CH3CHO | |
| C£® | ŗĻ³ÉČ«½µ½ā¾ŪĢ¼Ėįõ„ĖÜĮĻ£ŗ +nCO2$\stackrel{“߻ƼĮ}{”ś}$ +nCO2$\stackrel{“߻ƼĮ}{”ś}$ | |
| D£® | ŗĻ³ÉÓŠ»ś²£Į§µ„Ģå-¼×»ł±ūĻ©Ėį¼×õ„£ŗµŚŅ»²½£ŗ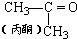 +HCN”ś£ØCH3£©2C£ØOH£©CN +HCN”ś£ØCH3£©2C£ØOH£©CNµŚ¶ž²½£ŗ£ØCH3£©2C£ØOH£©CN+CH3OH+H2SO4”ś  +NH4HSO4 +NH4HSO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 3ÖÖ | B£® | 4ÖÖ | C£® | 5ÖÖ | D£® | 6ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | õ„µÄĖ®½ā£¬õ„»Æ·“Ó¦£¬ŅŅ“¼ŗĶĒāĀ±Ėį·“Ó¦£¬ŅŅ“¼ŗĶÅØĮņĖįŌŚ140”ꏱ¼ÓČČ | |
| B£® | ±½Ļõ»Æ£¬±½ŗĶĒāĘų·“Ó¦£¬Ōķ»Æ·“Ó¦ | |
| C£® | µķ·ŪŌŚĮņĖį“ęŌŚĻĀÖĘĘĻĢŃĢĒ£¬Č©µÄŃõ»Æ»ņ»¹Ō | |
| D£® | ĻĖĪ¬ĖŲĖ®½ā£¬ÅØĮņĖįŗĶŅŅ“¼ŌŚ170”ꏱµÄ·“Ó¦£¬µ°°×ÖŹĖ®½ā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³ōŃõ | B£® | Ņ»Ńõ»ÆĢ¼ | C£® | µŖŃõ»ÆĪļ | D£® | Ģ¼Ēā»ÆŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀ³£Ń¹ĻĀ£¬22.4 LŅŅĻ©ÖŠŗ¬C-H¼üµÄŹżÄæĪŖ4NA | |
| B£® | 1molFeÓė×ćĮæŃĪĖį·“Ó¦×ŖŅʵē×ÓŹżĪŖ3NA | |
| C£® | 1.6gÓÉŃõĘųŗĶ³ōŃõ×é³ÉµÄ»ģŗĻĪļÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżÄæĪŖ0.1NA | |
| D£® | Ļņ1L 1 mol•L-1ĀČ»ÆĀĮČÜŅŗÖŠ¼ÓČė×ćĮæµÄ°±Ė®£¬Éś³ÉAlO2-µÄøöŹżĪŖNA |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com