
| A£® | Ąė×Ó»ÆŗĻĪļNH4ClÖŠ¼Č“ęŌŚĄė×Ó¼ü£¬ÓÖ“ęŌŚ¼«ŠŌ¹²¼Ū¼ü | |
| B£® | H2SµÄµē×ÓŹ½ŹĒ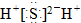 | |
| C£® | »Æѧ¼ü°üĄØĄė×Ó¼ü”¢¹²¼Ū¼ü”¢Ēā¼üµČ | |
| D£® | LiOH”¢NaOH”¢KOHµÄ¼īŠŌÖš½„¼õČõ |
·ÖĪö A£®ļ§øłĄė×ÓŗĶĖįøłĄė×ÓÖ®¼ä“ęŌŚĄė×Ó¼ü”¢²»Ķ¬·Ē½šŹōŌŖĖŲÖ®¼äŅ׊Ī³É¼«ŠŌ¼ü£¬ŗ¬ÓŠĄė×Ó¼üµÄ»ÆŗĻĪļŹĒĄė×Ó»ÆŗĻĪļ£»
B£®Įņ»ÆĒāŹĒ¹²¼Ū»ÆŗĻĪļ£¬Ō×ÓÖ®¼ä“ęŌŚ¹²¼Ū¼ü£»
C£®»Æѧ¼ü°üŗ¬Ąė×Ó¼ü”¢¹²¼Ū¼üŗĶ½šŹō¼ü£»
D£®ŌŖĖŲµÄ½šŹōŠŌŌ½Ē棬Ęä×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ¼īŠŌŌ½Ē森
½ā“š ½ā£ŗA£®ļ§øłĄė×ÓŗĶĀČĄė×ÓÖ®¼ä“ęŌŚĄė×Ó¼ü”¢N-HŌ×ÓÖ®¼ä“ęŌŚ¼«ŠŌ¼ü£¬ŗ¬ÓŠĄė×Ó¼üµÄ»ÆŗĻĪļŹĒĄė×Ó»ÆŗĻĪļ£¬øĆĪļÖŹÖŠŗ¬ÓŠĄė×Ó¼ü£¬ĪŖĄė×Ó»ÆŗĻĪļ£¬¹ŹAÕżČ·£»
B£®Įņ»ÆĒāŹĒ¹²¼Ū»ÆŗĻĪļ£¬Ęäµē×ÓŹ½ĪŖ £¬¹ŹB“ķĪó£»
£¬¹ŹB“ķĪó£»
C£®»Æѧ¼ü°üŗ¬Ąė×Ó¼ü”¢¹²¼Ū¼üŗĶ½šŹō¼ü£¬Ēā¼üŹōÓŚ·Ö×Ó¼ä×÷ÓĆĮ¦¶ų²»ŹōÓŚ»Æѧ¼ü£¬¹ŹC“ķĪó£»
D£®ŌŖĖŲµÄ½šŹōŠŌŌ½Ē棬Ęä×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ¼īŠŌŌ½Ē棬½šŹōŠŌK£¾Na£¾Li£¬ĖłŅŌ¼īŠŌLiOH£¼NaOH£¼KOH£¬¹ŹD“ķĪó£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²é»Æѧ¼ü”¢µē×ÓŹ½µÄŹéŠ“µČÖŖŹ¶µć£¬ĪŖøßĘµæ¼µć£¬²ąÖŲæ¼²éѧɜ·ÖĪöÅŠ¶ĻÄÜĮ¦£¬×¢Ņā»Æѧ¼üŗĶĒā¼üµÄ¹ŲĻµ¼°Ąė×Ó»ÆŗĻĪļŗĶ¹²¼Ū»ÆŗĻĪļµÄĒų±š£¬ŅדķŃ”ĻīŹĒC£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ō×Ó°ė¾¶°“X”¢Y”¢ZµÄĖ³ŠņŌö“ó | B£® | Ō×ÓŠņŹż°“X”¢Y”¢ZĖ³ŠņŌö“ó | ||
| C£® | µ„ÖŹµÄŃõ»ÆŠŌ°“X”¢Y”¢ZĖ³ŠņŌöĒæ | D£® | Ēā»ÆĪļµÄĪČ¶ØŠŌ°“X”¢Y”¢ZĖ³ŠņŌöĒæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ĪļÖŹ£ØĄØŗÅÄŚĪŖŌÓÖŹ£© | ³żŌÓŹŌ¼Į | ·½·Ø |
| A | äå±½£Øä壩 | CCl4 | ·ÖŅŗ |
| B | Ļõ»ł±½£ØHNO3£© | NaOH | ·ÖŅŗ |
| C | ŅŅĶé£ØŅŅĻ©£© | ĒāĘų | Ļ“Ęų |
| D | ŅŅ“¼£ØŅŅĖį£© | NaOH | ·ÖŅŗ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ū¢Ü¢Ż¢ą | B£® | ¢Ü¢Ż¢ß | C£® | ¢Ü¢Ż | D£® | ¢Ū¢Ü¢Ż¢ß¢ą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ō×Ó°ė¾¶Y£¾Z£¾X£¾W | B£® | Ēā»ÆĪļµÄĪČ¶ØŠŌH2Y£¾HZ | ||
| C£® | Ąė×ÓµÄŃõ»ÆŠŌaW3+£¾bX+ | D£® | a+3£¼c-2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO2ŗĶSiO2 | B£® | C60ŗĶAr | C£® | NaClŗĶHCl | D£® | CaOŗĶCsCl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŗ£“ųÖŠµāµÄĢįČ”ŹµŃéÖŠ£¬½«ŗ£“ų»ŅČÜÓŚĖ®£¬¹żĀĖŗóŌŚĀĖŅŗÖŠ¼ÓČėCCl4¼“æÉŻĶČ” | |
| B£® | ¼õŃ¹¹żĀĖæÉŅŌ¹żĀĖ½ŗד³Įµķ»ņæÅĮ£Ģ«Š”µÄ³Įµķ | |
| C£® | æÉĶعż¹Ū²ģĮņ“śĮņĖįÄĘČÜŅŗŗĶĮņĖį·“Ó¦²śÉśĘųĢåµÄæģĀżĄ“±Č½Ļ»Æѧ·“Ó¦ĖŁĀŹµÄæģĀż | |
| D£® | ŌŚ”°¶ĘŠæĢśĘ¤ŗń¶Č²āĮæ”±ŹµŃéÖŠ£¬µ±ŠæŌŚĖįÖŠĶźČ«Čܽāŗ󣬲śÉśĒāĘųµÄĖŁĀŹ»įĻŌÖų¼õĀż£¬æɽč“ĖÅŠ¶Ļ¶ĘŠæĢśĘ¤ÖŠŠæ¶Ę²ćŹĒ·ńĶźČ«·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “æ¼īČÜŅŗæÉČ„³żÓĶĪŪ | |
| B£® | NaClæÉÓĆ×÷·ĄøƼĮŗĶµ÷Ī¶¼Į | |
| C£® | ÅŻÄĆš»šĘ÷µÄĆš»šŌĄķ | |
| D£® | FeCl3±„ŗĶČÜŅŗµĪČė·ŠĖ®ÖŠÖĘFe£ØOH£©3½ŗĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com