
����ͼ��ʾ����ԲȦ�ཻ�IJ��ֱ�ʾԲȦ�ڵ�����������ķ�Ӧ����֪�Ƽ�������������ʵ�����Ϊ0.1mol��ˮ������Ϊ100g������˵����ȷ���ǣ���
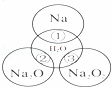
A�� ��Ӧ������ܲ���0.05mol O2
B�� ��Ӧ�ٵ����ӷ���ʽΪ��Na+2H2O═Na++2OH﹣+H2��
C�� Na2O2������������Ŀ֮��Ϊ1��1
D�� �١��ڡ��۳�ַ�Ӧ��������Һ�����������Ӵ�С���٣��ڣ���
���㣺 �ƵĻ�ѧ���ʣ���ѧ����ʽ���йؼ��㣻�Ƶ���Ҫ�����
ר�⣺ ������Ҫ�Ľ������仯���
������ A�����ݹ������ƺ�ˮ��Ӧ�ķ���ʽ�����������������ʵ�����
B�����ӷ���ʽҪ��ѭ��ԭ���غ�͵���غ�ȡ����ɣ�
C�����������е��������ǹ��������Ӳ��������ӣ����ݻ�ѧʽ����֮�ȣ�
D�����ݹ�������ʵ���������Һ�����ʵ���������Һ����������������������ʽ�ж�����������Դ�С��
��� �⣺A����Ӧ�ۣ�2Na2O2+2H2O=4NaOH+O2����
2mol 1mol
0.1mol 0.05mol
���ݷ���ʽ֪��������0.05molO2����A��ȷ��
B��Na+2H2O═Na++2OH﹣+H2���е�ɲ��غ㣬��Ӧ����ȷ�����ӷ���ʽΪ��2Na+2H2O=2Na++2OH﹣+H2������B����
C��������������������O2 2﹣����������������Ŀ֮��Ϊ1��2����C����
D���ơ������ơ��������ƺ�ˮ��Ӧ�ķ���ʽ�ֱ����£�
Na+H2O=NaOH+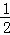 H2������Һ���ӵ�����=m��Na��﹣m��H2��=2.3g﹣0.1g=2.2g��
H2������Һ���ӵ�����=m��Na��﹣m��H2��=2.3g﹣0.1g=2.2g��
Na2O+H2O=2NaOH����Һ���ӵ�����=m��Na2O��=0.1mol��62g/mol=6.2g��
Na2O2+H2O=2NaOH+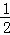 O2������Һ���ӵ�����=m��Na2O2��﹣m��O2��=m��Na2O��=6.2g
O2������Һ���ӵ�����=m��Na2O2��﹣m��O2��=m��Na2O��=6.2g
������Һ���ӵ�������С˳��Ϊ���ƣ�������=�������ƣ�
������ԭ���غ�֪��0.1mol���ơ������ơ��������ơ�����ˮ�����������Ƶ����ʵ����ֱ�Ϊ��0.1mol��0.2mol��0.2mol��ͨ�����Ϸ�����֪��0.1mol���ơ������ơ��������ơ��ֱ�����ˮ������Һ�����������ֱ�Ϊ��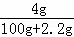 ��
�� ��
�� �����Ԣ١��ڡ��۳�ַ�Ӧ��������Һ�����������Ӵ�С���٣���=�ۣ���D����
�����Ԣ١��ڡ��۳�ַ�Ӧ��������Һ�����������Ӵ�С���٣���=�ۣ���D����
��ѡA��
������ ���⿼�����Ƽ��仯��������ʣ������������������ǹ��������Ӳ��������ӣ�Ϊ�״��㣬ע��֪ʶ�Ĺ��ɺ������Լ����Ӧ���ǹؼ����ѶȲ���


 ���źþ���Ԫ����ĩ��ϵ�д�
���źþ���Ԫ����ĩ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼΪϡ��Ԫ���棨Ce����Ԫ�����ڱ��е������Ϣ������˵��������ǣ�������

| �� | A�� | ���ԭ������Ϊ58 | B�� | �����ڽ���Ԫ�� |
| �� | C�� | ��ԭ���е�������Ϊ58 | D�� | ��ԭ�ӵ�����Ϊ140.1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������A�����ϣ��������������֪����Է�������Ϊ136������ʽΪC8H8O2��A�ĺ˴Ź���������4���������֮��Ϊ1��2��2��3��A������ֻ��һ�������ұ�����ֻ��һ��ȡ����������������˴Ź�����������ͼ������A������˵���У���ȷ���ǣ���

A�� ��A����ͬ������ͬ���칹��ֻ��2��
B�� A��һ�������¿���4 mol H2�����ӳɷ�Ӧ
C�� A����������������һ�������²��ܷ���ˮ�ⷴӦ
D�� ��������A���ӽṹ�������л���ֻ��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��һ����Ϣ���ϵ����Ӽ�������ͬ�����£�A������������ͬ�������������88.25������A�����и�Ԫ�����������ֱ�Ϊw��C��=54.4%��w��H��=7.4%��w��O��=18.1%��w��Cl��=20.1%��A�ڲ�ͬ�����¿ɷ�����ͼ��ʾ��һϵ�б仯��
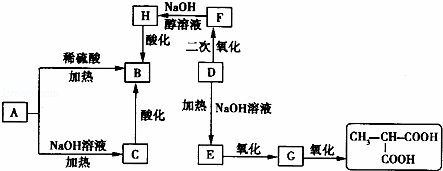
��ش��������⣺
��1��A�ķ���ʽΪ ��
��2��D���Ӻ��еĹ������� ��
��3������ת����ϵ�Ļ�ѧ����ʽ�У�����ˮ�ⷴӦ���� ���������֣���
��4��д����ѧ����ʽ��
��A��ϡ���Ṳ�ȣ� ��
��E������G�� ��
��F���������ƴ���Һ���ȣ� ��
��5����B��Ϊͬ���칹�����������״�������ʹ��� �֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵���в���ȷ���ǣ���
A�� ��״���£��������CH4��CO2�������õ��Ӷ������
B�� ��NaOH��Һ��H2SO4��Һ��Ӧ��������H2�����������������
C�� 1 mol OH﹣��17 g NH3�������������
D�� ������Һ��K+��Al3+���ʵ���Ũ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
FeCl3��CuCl2�Ļ����Һ�м������ۣ���ַ�Ӧ�����й�����ڣ��������жϲ���ȷ���ǣ���
A�� ����KSCN��Һһ�������ɫ B�� ��Һ��һ����Fe2+
C�� ��Һ��һ������Cu2+ D�� ʣ�������һ����Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Ӧ��A+3B⇌2C+D�������ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ��
��vA=0.15mol•L﹣1min﹣1
��vB=0.6mol•L﹣1min﹣1
��vC=0.4mol•L﹣1min﹣1
��vD=0.45mol•L﹣1min﹣1
�÷�Ӧ���е������ǣ�������
| �� | A�� | �� | B�� | �� | C�� | �٢� | D�� | �ڢ� |
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
1���pH=2.5��������10���ijһԪǿ����Һǡ����ȫ��Ӧ���Ǹü���Һ��pH���ڣ�������
| �� | A�� | 9.0 | B�� | 9.5 | C�� | 10.5 | D�� | 11.0 |
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ԫ�صĻ�ѧ������Ҫ������ԭ�ӵģ���
A�� ������ B�� ������ C�� ��������� D�� ����������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com