
【题目】向NaOH和Na2CO3混合溶液中滴加0.1mol/L盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示,下列判断正确的是( )
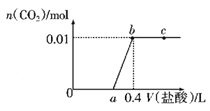
A. a点时溶液中存在c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
B. 0~a段溶液中水电离出的OH-浓度先增大后减小
C. a=0.2
D. ab段发生反应的离子方程式为CO32-+2H+=H2O+CO2↑
【答案】B
【解析】对NaOH和Na2CO3混合配成的溶液,当滴加盐酸时,先发生氢氧化钠与盐酸的中和反应,再发生碳酸钠与盐酸的反应生成碳酸氢钠和氯化钠,最后发生碳酸氢钠与盐酸反应才有二氧化碳气体生成。A. a点时溶液中存在氯化钠,碳酸氢钠,根据物料守恒,c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)+ c(Cl-),故A错误;B. 0~a段溶液中先发生氢氧化钠与盐酸的中和反应,溶液中氢氧化钠逐渐减少,水的电离程度逐渐增大,再发生碳酸钠与盐酸的反应生成碳酸氢钠和氯化钠,碳酸钠的水解程度大于碳酸氢钠,水的电离程度又逐渐减小,因此水电离出的OH-浓度先增大后减小,故B正确;C、根据碳元素守恒,混合物中,碳酸钠的物质的量是0.01mol,所以两步反应:HCl+Na2CO3=NaHCO3+NaCl,NaHCO3+HCl=NaCl+H2O+CO2↑,分别消耗的盐酸的量是0.01mol,0.1molL-1稀盐酸的体积分别是0.1L,所以a=0.3,故C错误; D、ab段发生反应为:NaHCO3+HCl=NaCl+H2O+CO2↑,反应的离子方程式为:HCO3-+H+=H2O+CO2↑,故D错误;故选B。


科目:高中化学 来源: 题型:
【题目】能源是当今社会发展的三大支柱之一.根据题中提供的信息,请回答下列问题:
I.天然气和甲醇都是一种高效、低耗、污染小的清洁能源。在一定条件下,通过太阳光的作用,形成如图所示的物质循环。
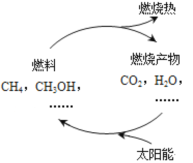
(1)写出甲烷完全燃烧的化学方程式________
(2)如图的物质循环中太阳能最终转化为_________能。
II.新冠疫情防控期间,测温枪发挥了极大的作用。有一种便携式测温枪,里面使用了锌银纽扣式电池,其电极材料分别为Zn和Ag2O,电解质为KOH溶液。工作时电池总反应为:Zn+ Ag2O+H2O=2Ag+ Zn(OH)2
(3)正极的电极反应式为___________
(4)外电路每通过0.4 mole-,负极质量增重了______ g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下
CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下
A. 加入催化剂,改变了反应的途径,反应的ΔH也随之改变
B. 增大压强,正逆反应的化学反应速率都减小
C. 升高温度, 正反应化学反应速率增大, 逆反应化学反应速率减小
D. 对该反应来说,无论反应进行到何时,混合气体的总物质的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铁矿石是制取硫酸的主要原料,主要成分为FeS2和少量FeS(假设其它杂质中不含铁、硫元素,且高温下不发生化学变化)。某化学兴趣小组对该黄铁矿石进行如下实验探究。将m1g该黄铁矿石的样品放入如图装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全。其反应的化学方程式为4FeS2+11O2=2Fe2O3+8SO2,4FeS+7O2=2Fe2O3+4SO2

(1)鼓人空气的作用是___________,锥形瓶乙中NaOH溶液的作用是___________。
(实验一)测定硫元素的含量
反应结束后,将乙瓶中的溶液进行如下处理:

(2)反应结束后,给乙瓶溶液中加入足量H2O2溶液的目的是___________(用化学方程式表示)。
(3)洗涤滤渣的方法是______________________。
(4)该黄铁矿石中硫元素的质量分数为___________(列出表达式即可)。
(实验二)测定铁元素的含量
①用足量稀硫酸溶解石英管中的固体残渣;②加还原剂使溶液中的Fe3+恰好完全转化为Fe2+后,过滤、洗涤;③将滤液稀释至250mL;④取25.00mL稀释液,用0.1000mol·L-1的酸性KMnO4溶液滴定,三次滴定实验,平均消耗酸性KMnO4溶液25.00mL。
(5)操作②中用铁粉作还原剂,测定铁的含量___________(填“偏高”或“偏低”或“不变”),操作④中滴定时酸性KMnO4溶液盛装在___________填“酸式滴定管”或“碱式滴定管”),③中稀释液中Fe2+的物质的量浓度c(Fe2+)=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)CH2=CH C(CH3) =CH2系统命名为:____________________________。
(2)写出“间甲基苯乙烯”的结构简式 :____________________________。
(3)在标准状况下,某烃的密度是1.25g·L-1,一定体积的该烃完全燃烧生成4.48LCO2和3.6g水,该烃的分子式_________________。
(4)有机物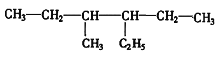 的正确命名_______________________。
的正确命名_______________________。
(5)现有下列5种有机物:
A、CH2=CH2
B、CH3C≡CH
C、CH3CH2CH2OH
D、CH3OCH2CH3
E、![]() 。
。
请回答:
属于烃类的是______(填序号,下同),与A互为同系物的是______,与C互为同分异构体的是______.用系统命名法给E命名,其名称为______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL的某稀H2SO4溶液中滴入0.1mol/L氨水,溶液中水电离出氢离子浓度随滴入氨水体积变化如图。下列分析正确的是
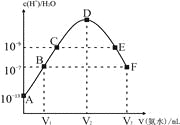
A.E溶液中存在:c(NH4+)>c(SO42-)> c(OH-)> c(H+)
B.稀硫酸的浓度为0.1mol/L
C.C点溶液pH=14-b
D.V2=20mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇燃料电池由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注,其工作示意图如下,其总反应为 2CH3OH+3O2===2CO2+4H2O。下列说法不正确的是( )

A. 电极 A 是负极,物质 a 为甲醇
B. 电池工作时,电解液中的 H+通过质子交换膜向 B 电极迁移
C. 放电前后电解质溶液的 pH 增大
D. b 物质在电极上发生的电极反应式为: O2+4eˉ+2H2O=4OHˉ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以链烃A为原料合成两种高分子材料的路线如下图所示:
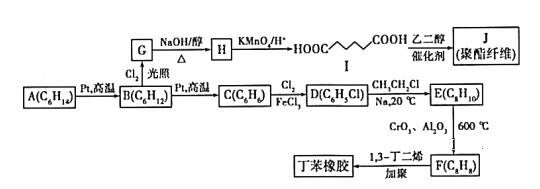
已知以下信息:①分子式A(C6H14)、B(C6H12) 、C(C6H6) 、D(C6H5Cl) 、E(C8H10) 、F(C8H8)
②B(C6H12)的核磁共振氢谱中只有1组峰,G为一氯代烃;
③R1-X+R2-X ![]() R1- R2 (X代表卤素原子,R1、R2代表烃基)。
R1- R2 (X代表卤素原子,R1、R2代表烃基)。
④![]()
![]()
![]() +R3-COOH(R1、R2、R3代表烃基)。
+R3-COOH(R1、R2、R3代表烃基)。
请回答以下问题:
(1) B的化学名称为______________________。
(2)由G生成H的化学方程式为_____________________。
(3)由C生成D的反应类型为_____________。
(4)F的结构简式为_________________。
(5)I的同分异构体中能同时满足下列条件的共有____________种(不含立体异构)。
①能与饱和NaHCO3溶液反应产生气体;②既能发生银镜反应,又能发生水解反应。其中核磁共振氢谱中有4组峰,且峰面积之比为6:2:1:1的是________(写出其中一种的结构简式)。
(6)参照上述合成路线,以2-甲基己烷和一氯甲烷为原料(无机试剂任选),设计制备化合物E的合成路线___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D四种物质都是气体,现在5L的密闭容器中进行反应:4A+5B![]() 4C+6D,30s后C的物质的量增加了0.30mol。则下列有关叙述正确的是( )
4C+6D,30s后C的物质的量增加了0.30mol。则下列有关叙述正确的是( )
A.反应开始至30s,v(A)=0.010mol·L-1·s-1
B.30s时容器中D的物质的量至少为0.45mol
C.30s时容器中A、B、C、D的物质的量之比一定是4∶5∶4∶6
D.反应开始至30s,容器中A的物质的量增加了0.30mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com