
已知NaOH+Al(OH)3→NaAlO2。向集满CO2的铝制易拉罐中加入过量NaOH浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。上述实验过程中没有发生的离子反应是( )
A.CO2+2OH?→CO32?+H2O B.Al2O3+2OH?→2 AlO2 ? +H2O
C.2 Al+2OH?+2H2O→2 AlO 2 ?+3 H2↑ D.Al3++4 OH?→AlO2? +2H2O
2 ?+3 H2↑ D.Al3++4 OH?→AlO2? +2H2O
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 分别加入适量澄清石灰水 | B. | 分别滴加紫色石蕊试液 | ||
| C. | 分别将带火星的木条伸入瓶中 | D. | 分别将燃着的木条伸入瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2017届海南省高三上学期月考三化学试卷(解析版) 题型:选择题
赏心悦目的雕花玻璃是用下列哪种物质对普通玻璃进行刻蚀而制成的,该物质是( )
A.氢硫酸 B. 氢氟酸 C.浓硫酸 D.浓硝酸
查看答案和解析>>
科目:高中化学 来源:2017届广西桂林十八中高三上10月月考化学试卷(解析版) 题型:选择题
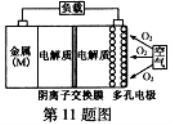
金属(M)–空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH) n。已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是( )
A.采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于 氧气扩散至电极表面
氧气扩散至电极表面
 B.比较Mg、Al、Zn三种金属–空气电池,Al–空气电池的理论比能量最高
B.比较Mg、Al、Zn三种金属–空气电池,Al–空气电池的理论比能量最高
C.M–空气电池放电过程的正极反应式:4Mn++nO2+2nH2O+4ne–=4M(OH)n
D.在M–空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
查看答案和解析>>
科目:高中化学 来源:2017届广西桂林十八中高三上10月月考化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.常温常压下,22.4L Cl2中含有的分子数为6.02×1023个
B.0.1mol/LNa2CO3溶液加热后,溶液的pH减小
C.氢氧燃料电池工作时,H2在负极上失去电子
D.室温下,稀释0.1mol/LCH3COOH溶液,溶液的导电能力增强
查看答案和解析>>
科目:高中化学 来源: 题型:解答题



查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硫代硫酸钠(Na2S2O3)可用做分析试剂及鞣革还原剂.它受热、遇酸易分解.工业上可用反应:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示.(说明:a中盛放稀硫酸;b中盛放Na2SO3固体)回答下列问题:
硫代硫酸钠(Na2S2O3)可用做分析试剂及鞣革还原剂.它受热、遇酸易分解.工业上可用反应:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示.(说明:a中盛放稀硫酸;b中盛放Na2SO3固体)回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com