
【题目】过氧化氢的沸点比水高,但受热容易分解。某试剂厂先制得7~8%的过氧化氢溶液,再浓缩成30%的溶液时,可采用的适宜方法是( )
A.常压蒸馏
B.减压蒸馏
C.加生石灰常压蒸馏
D.加压蒸馏
科目:高中化学 来源: 题型:
【题目】下列液体中,不会出现丁达尔效应的分散系是( )
①鸡蛋白溶液 ②水 ③淀粉溶液 ④硫酸钠溶液 ⑤Fe(OH)3胶体
A. ②④ B. ①③ C. ③⑤ D. ④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用压强传感器探究生铁在pH=2和pH=4醋酸溶液中发生腐蚀的装置及得到的图象如下:分析图象,以下结论错误的是( ) 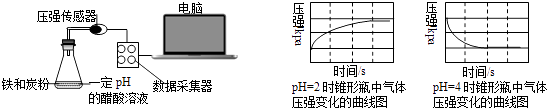
A.溶液pH≤2时,生铁发生析氢腐蚀
B.在酸性溶液中生铁可能发生吸氧腐蚀
C.析氢腐蚀和吸氧腐蚀的速率一样快
D.两溶液中负极反应均为:Fe﹣2e﹣═Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把500 mL NH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含a mol氢氧化钠的溶液恰好反应完全,另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为( )
A. (![]() -
-![]() ) mol/L B. (2b-a) mol/L
) mol/L B. (2b-a) mol/L
C. (5b-![]() ) mol/L D. (10b-5a) mol/L
) mol/L D. (10b-5a) mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不用其它任何试剂鉴别下列5种物质的溶液:①KOH ②MgSO4 ③Ba(NO3)2 ④CuCl2 ⑤KNO3,被鉴别出来的正确顺序是
A. ⑤④③②① B. ④①②③⑤ C. ②③①④⑤ D. ④①⑤②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重要的化学品M和N的合成路线如图所示: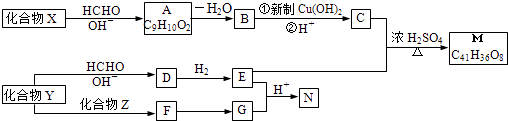
已知:i. ![]()
ii. ![]()
iiiN的结构简式是: 
请回答下列问题:
(1)A中含氧官能团名称是 , C 与E生成M的反应类型是 .
(2)写出下列物质的结构简式:X:Z:E:
(3)C和甲醇反应的产物可以发生聚合反应.该聚合反应的产物是: .
(4)1molG一定条件下,最多能与mol H2发生反应
(5)写出一种符合下列要求G的同分异构体①有碳碳叄键 ②能发生银镜反应 ③一氯取代物只有2种
(6)1,3﹣丙二醇是重要的化工物质,请设计由乙醇合成它的流程图合成路线流程图示例如下:CH2=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH.
CH3CH2OH.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化钠是一种重要的化工原料.工业上用硫酸钠来制得硫化钠.制备硫化钠的反应原理为:Na2SO4(s)+4H2(g)Na2S(s)+4H2O(g)﹣Q,已知该可逆反应在1000℃时达到平衡,并保持反应器内恒温恒容.试回答下列问题:
(1)此可逆反应的平衡常数表达式可表示为 , 若只改变一个影响因素,当平衡移动时,K值变化(填“一定”或“不一定”);当K值变大时,逆反应速率 . (填“增大”、“减小”或“不变”)
(2)该反应达到平衡时下列说法错误的是 . a.容器内压强保持不变
b.氢气和水蒸汽的物质的量之比保持不变
c.加入少量Fe3O4固体,平衡向逆反应方向移动
d.移除部分Na2S固体,平衡向正反应方向移动
(3)该温度下,在2L盛有2.84g Na2SO4的密闭容器中通入H2气体,10分钟后测得固体质量为2.264g.则10分钟内H2的平均反应速率为 .
(4)往Ba(ClO)2溶液中通入足量SO2气体后,溶液中的溶质是 .
(5)向亚硫酸钠中滴加酚酞,溶液变为红色,若在该溶液中再滴入过量的BaCl2溶液,现象是 , 请结合离子方程式,运用平衡原理进行解释: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图5个装置都是中学化学中常见的实验装置,某学习小组的同学欲用这些装置进行常见物质的制取并探究其性质(图中a、b、c表示止水夹),请对其进行完善或评价,试回答下列问题:
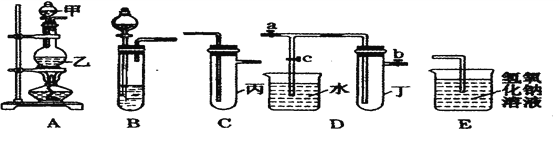
(1)将A、C、E相连后,以浓盐酸和_______(填写名称)为原料制取Cl2,仪器乙的名称是________。写出实验中制备氯气的离子方程式___________________。
(2)利用(1)中装置和药品,在丙中加入适量水,即可制得氯水。将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验实验操作、现象、结论如下:
实验序号 | 实验操作 | 现象 | 结论 |
Ⅰ | 将所得氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物有漂白性 |
Ⅱ | 向所得氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应至少产生一种酸性强于碳酸的物质 |
实验Ⅰ获得结论是否合理?_________(填“合理”或“不合理”)。若选“不合理”,请说明理由(若选“合理”,则无需填写理由):___________________________________________。
实验Ⅱ获得结论是否合理?_________(填“合理”或“不合理”)。若选“不合理”,请说明理由(若选“合理”,则无需填写理由):______________________________________________。
(3)利用(1)中装置还可设计一个简单的实验比较Cl-和S2-的还原性强弱。则C中预期出现的现象是______________________________________________________________。
(4)将B、D、E装置相连接(打开止水夹a和止水夹b,关闭止水夹c),在B中盛装浓硝酸和铜片(将铜片放在有孔塑料板上),可制得NO2。一段时间后,欲用D装置探究NO2与水的反应,其操作步骤为:先______________________________,再____________________________以使烧杯中的水进入试管丁,观察现象。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇是生活中常接触到的一种有机化合物,请回答下列问题
(1)饭店中常使用固体酒精,你判断它应是(填混合物或纯净物),质量较差的固体酒精在使用时因燃烧不充分,可能产生有毒气体(写化学式);
(2)在焊接铜漆包线的线头时,常先把线头放在火上烧一下以除去漆层,并立即在酒精中蘸一下就可得光亮的铜线,这个过程中乙醇发生(填氧化反应或还原反应);
(3)乙醇和乙酸可以发生酯化反应,请写出化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com