
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如下图(其中I代表H2A,II代表HA-,III代表A2-) 根据图示判断,下列说法正确的是
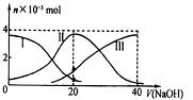
A.当V(NaOH)=20 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
B.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
C.欲使NaHA溶液呈中性,可以向其中加入酸或碱
D.向NaHA溶液加入水的过程中,pH可能增大也可能减少
科目:高中化学 来源:2016-2017学年宁夏高一上月考二化学卷(解析版) 题型:选择题
在一定条件下MnO4-与SO32-反应产物是Mn2+,则与1 mol MnO4-反应所需SO32-的物质的量为( )
A.3.0 mol B.2.5 mol C.1.0 mol D.0.75 mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上月考二化学卷(解析版) 题型:选择题
已知Zn(s)+H2SO4(aq)===ZnSO4(aq)+H2(g)ΔH<0,则下列叙述不正确的是( )
A.该反应中旧化学键断裂需要吸收能量,新化学键形成需要放出能量,所以反应前后物质具有的总能量不变
B.上述热化学方程式中的ΔH的值与实验测定中反应物的用量无关
C.该反应的化学能可以转化为其他形式的能
D.反应物的总能量高于生成物的总能量
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省沈阳东北育才学校高三上期中模拟化学卷(解析版) 题型:选择题
三种气体X、Y、Z的相对分子质量关系为Mr(X)<Mr(Y)=0.5Mr(Z),下列说法正确的是
A.原子数目相等的三种气体,质量最大的是Z
B.相同条件下,同质量的二种气体,气体密度最小的是X
C.若一定条件下,三种气体体积均为2.24 L,则它们的物质的量一定均为0.1mol
D.同温下,体积相同的两容器分别充2gY气体和l g Z气体,则其压强比为2:1
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上11.27周考化学卷(解析版) 题型:推断题
【化学——选修物质结构与性质】已知A、B、C、D、E五种元素的原子序数依次增大,其中A、E原子的最外层电子数均等于其周期序数,E原子的电子层数是A的3倍;B原子核外电子有6种不同的运动状态,S轨道电子数是P轨道电子数的两倍;D原子L层上有2对成对电子。请回答下列问题:
(1)E元素基态原子的电子排布式为___________________________。
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为_____________(填元素符号)。
(3)D元素与氟元素相比,电负性:D_______________F(填“>”、“=”或“<”)。
(4)BD2在高温高压下所形成的晶体其晶胞如图所示。该晶体的类型属于___________________(选填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中B原子轨道的杂化类型为_____________。l mol B2A2分子中含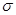 键的数目是_________________。
键的数目是_________________。

(5)光谱证实单质E与强碱溶液反应有[E(OH)4]—生成,则[E(OH)4]—中存在____________。
a.共价键 b.配位键 c.σ键 d.π键
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上11.27周考化学卷(解析版) 题型:选择题
升高温度,下列数据不一定增大的是
A.化学反应速率v B.水的离子积常数Kw
C.化学平衡常数K D.弱酸的电离平衡常数Ka
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上月考三化学卷(解析版) 题型:选择题
常温下,有下列四种溶液:①0.1 mol/L NaOH溶液 ②pH = 11 NaOH溶液 ③0.1 mol/L CH3COOH溶液 ④pH = 3 CH3COOH溶液 ⑤pH = 3 HCl溶液,下列说法正确的是( )
A.由水电离出H+的浓度c(H+):①>③
B.将等体积的④、⑤分别加蒸馏水稀释至pH = 6,加入水的体积:④>⑤
C.①与③混合,若溶液pH=7 ,则体积:V(NaOH)>V(CH3COOH)
,则体积:V(NaOH)>V(CH3COOH)
D.将②与④等体积混合,得到的溶液pH>7
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上半期考试化学卷(解析版) 题型:选择题
下列说法正确的是( )
A.BaSO4难溶于水,所以BaSO4不是电解质[
B.SO2溶于水所得溶液可以导电,所以SO2是电解质
C.分散系一定是混合物
D.电解质的电离需要通电才能进行
查看答案和解析>>
科目:高中化学 来源:2017届西藏山南二中高三上11月月考化学试卷(解析版) 题型:实验题
某研究性学习小组利用所示装置探究二氧化硫的性质。(装置中固定仪器未画出)

(1)A中所装试剂为铜片和 。(填试剂名称)。
(2)D中试剂为0.5 mol/L BaCl2溶液,实验中无明显现象,若改为同浓度的Ba(NO3)2溶液,则出现白色沉淀,此沉淀的化学式为 ,证明SO2具有 性。
(3)装置B用于验证SO2的漂白性,则其中所装溶液可以为 。
A.酸性高锰酸钾溶液 B.品红溶液 C.石蕊试液 D.蓝色的碘—淀粉溶液
(4)实验时,B中 溶液褪色,并有大量气泡冒出,但始终未见C中饱和澄清石灰水出现浑浊或沉淀。请推测可能原因,并设计实验验证。
溶液褪色,并有大量气泡冒出,但始终未见C中饱和澄清石灰水出现浑浊或沉淀。请推测可能原因,并设计实验验证。
可能原因: 。
实验验证: 。
(5)E中Na2S溶液用于验证SO2的氧化性,预期观察到的现象为  。
。
(6)指出上述装置中一处明显的不足: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com