
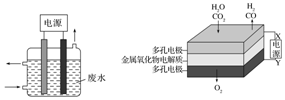
 用图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,阳极的电极反应式为:Cl-+2OH--2e-═ClO-+H2O;
用图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,阳极的电极反应式为:Cl-+2OH--2e-═ClO-+H2O;分析 根据装置图,该电解质溶液呈碱性,电解时,阳极要生成氯气,氯气和氢氧根离子反应生成次氯酸根离子和水,ClO-将CN-氧化为两种无污染的气体,两种气体为二氧化碳和氮气,据此分析.
解答 解:阳极上氯离子失电子生成氯气,氯气和氢氧根离子反应生成次氯酸根离子和水,所以阳极反应式为:Cl-+2OH--2e-═ClO-+H2O;
电解质溶液呈碱性,则阴极电极反应式为2H++2e-=H2↑;
阳极产生的ClO-将CN-氧化为两种无污染的气体,两种气体为二氧化碳和氮气,该反应在碱性条件下进行,所以应该有氢氧根离子生成,反应方程式为2CN-+5ClO-+H2O═N2↑+2CO2↑+5Cl-+2OH-;
故答案为:Cl-+2OH--2e-═ClO-+H2O;2H++2e-=H2↑;2CN-+5ClO-+H2O═N2↑+2CO2↑+5Cl-+2OH-.
点评 本题主要考查电解原理,明确各个电极上发生的反应及电解原理是解本题关键,注意D中碱性条件下不能有氢离子参加反应或生成.题目难度不大,是基础题.


科目:高中化学 来源: 题型:选择题
| A. | 可逆返应达到平衡的重要特征是正、逆反应速率都为零,反应停止了 | |
| B. | 在可逆反应里,正反应的速率是正值,逆反应的速率是负值 | |
| C. | 对于H2+I2 2HI,当有1molH-H键断裂的同时,有2molH-I键生成,说明此可逆反应已达化学平衡 2HI,当有1molH-H键断裂的同时,有2molH-I键生成,说明此可逆反应已达化学平衡 | |
| D. | 在一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物和生成物的浓度不再发生变化,表明该反应达到化学平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向生石灰中滴加浓氨水以制备纯净的氨气 | |
| B. | 用分液漏斗分离碘和四氯化碳 | |
| C. | 用排饱和硝酸钾溶液法收集铜与浓硝酸反应产生的NO | |
| D. | 向含Al3+的氯化镁溶液中加入过量MgO,过滤得到MgCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,A在一定条件下有如图所示的转化关系.
,A在一定条件下有如图所示的转化关系.
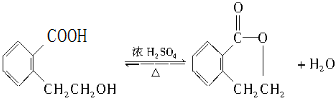 ,写出所有符合下列要求的E的同分异构体的结构简式:
,写出所有符合下列要求的E的同分异构体的结构简式: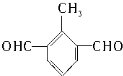 、
、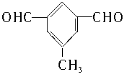 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
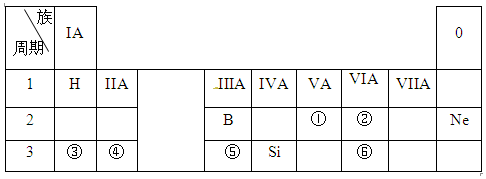
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ||||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
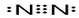 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解时在电解池的阳极上不一定有阴离子放电 | |
| B. | 原电池跟电解池连接后,电子从原电池负极流向电解池阳极 | |
| C. | 电解池是将电能转化为化学能的装置 | |
| D. | 电解时,电源负极流出的电子数等于流入电源正极的电子数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com