
| A£® | ŅŌÉĻ·“Ó¦¾łæÉ·¢Éś | B£® | Ö»ÓŠ¢ß²»ÄÜ·¢Éś | ||
| C£® | Ö»ÓŠ¢Ž²»ÄÜ·¢Éś | D£® | Ö»ÓŠ¢Ś²»ÄÜ·¢Éś |
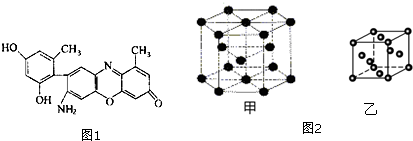
·ÖĪö øĆ·Ö×ÓÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼üŗĶ-ClŌ×Ó£¬¾ßÓŠĻ©Ģž”¢ĀČ“śĢžµÄŠŌÖŹ£¬¾Ż“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗøĆ·Ö×ÓÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼üŗĶ-ClŌ×Ó£¬¾ßÓŠĻ©Ģž”¢ĀČ“śĢžµÄŠŌÖŹ£¬
Ģ¼Ģ¼Ė«¼üÄÜ·¢Éś¼Ó³É·“Ó¦”¢»¹Ō·“Ó¦”¢Ńõ»Æ·“Ó¦”¢¼Ó¾Ū·“Ó¦£¬ÄÜŗĶäå·¢Éś¼Ó³É·“Ó¦¶ųŹ¹äåĖ®ĶŹÉ«£¬Äܱ»ĖįŠŌøßĆĢĖį¼ŲČÜŅŗŃõ»Æ¶ųŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«£»
ŗ¬ÓŠĀČŌ×Ó£¬ĖłŅŌÄÜ·¢ÉśČ”“ś·“Ó¦”¢ĻūČ„·“Ó¦£¬ŅņĪŖ²»ÄܵēĄė³ö×ŌÓÉŅĘ¶ÆµÄĀČĄė×Ó£¬ĖłŅŌ²»ÄÜŗĶĻõĖįŅųČÜŅŗ·“Ó¦£¬¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļ½į¹¹ŗĶŠŌÖŹ£¬ĪŖøßĘµæ¼µć£¬Ć÷Č·¹ŁÄÜĶż°ĘäŠŌÖŹ¹ŲĻµ¼“æɽā“š£¬²ąÖŲæ¼²éĀ±“śĢž”¢Ļ©ĢžŠŌÖŹ£¬×¢ŅāĀČ“śĢž·¢ÉśĻūČ„·“Ó¦Ź±ĀČ“śĢž½į¹¹ĢŲµć£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ²Ł×÷ | ĻÖĻó |
| ĻņŹ¢ÓŠ4g””Na2O2µÄÉÕ±ÖŠ¼ÓČė50mLÕōĮóĖ®µĆµ½ČÜŅŗa | ¾ēĮŠ·“Ó¦£¬²śÉśÄÜŹ¹“ų»šŠĒľĢõø“Č¼µÄĘųĢå |
| Č”5mLČÜŅŗaÓŚŹŌ¹ÜÖŠ£¬µĪČėĮ½µĪ·ÓĢŖ | ¢”£®ČÜŅŗ±äŗģ ¢¢£®10·ÖÖÖŗóČÜŅŗŃÕÉ«Ć÷ĻŌ±äĒ³£¬ÉŌŗó£¬ČÜŅŗ±äĪŖĪŽÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1molĀČĘų²Ī¼ÓŃõ»Æ»¹Ō·“Ó¦£¬×ŖŅʵĵē×ÓŹżŅ»¶ØĪŖ2 NA | |
| B£® | 0.1mol FeÓė0.1mol Cl2³ä·Ö·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ0.3NA | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ£¬44g¶žŃõ»ÆĢ¼·Ö×ÓÖŠĖłŠĪ³ÉµÄ¹²ÓƵē×Ó¶ŌŹżĪŖ2 NA | |
| D£® | ³£ĪĀ³£Ń¹ĻĀ£¬1.6gO2ŗĶO3»ģŗĻĘųĢåÖŠÖŹ×Ó×ÜŹżĪŖ0.8NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĻ©£ØCH2=CH2£©”¢±½£Ø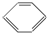 £©”¢»·¼ŗĶé£Ø £©”¢»·¼ŗĶé£Ø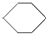 £©¶¼ŹōÓŚÖ¬·¾Ģž £©¶¼ŹōÓŚÖ¬·¾Ģž | |
| B£® | ±½£Ø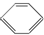 £©”¢»·ĪģĶé£Ø £©”¢»·ĪģĶé£Ø £©”¢»·¼ŗĶé£Ø £©”¢»·¼ŗĶé£Ø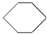 £©Ķ¬ŹōÓŚ·¼ĻćĢž £©Ķ¬ŹōÓŚ·¼ĻćĢž | |
| C£® | ŅŅĻ©£ØCH2=CH2£©”¢ŅŅČ²£ØCH”ŌCH£©Ķ¬ŹōÓŚĻ©Ģž | |
| D£® | 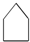 ”¢ ”¢ ”¢ ”¢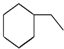 Ķ¬ŹōÓŚ»·ĶéĢž Ķ¬ŹōÓŚ»·ĶéĢž |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com