
【题目】某研究小组利用“钯催化交叉偶联反应”合成了有机物丙,合成路线如下:
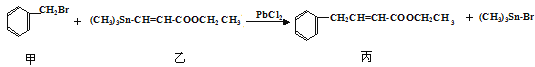
列下分析判断正确的是( )
A.分离提纯有机物丙宜在NaOH热溶液中进行
B.利用NaOH溶液、AgNO3溶液即可确定有机物甲中含有溴元素
C.可用酸性KMnO4溶液检验有机物丙中是否含有机物乙
D.PbCl2的作用是提高反应物的活性,加快反应速率
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可实现燃煤烟气中硫的回收:2CO(g)+SO2(g)![]() 2CO2(g)+S(l) ΔH
2CO2(g)+S(l) ΔH
(1)已知:2CO(g)+O2(g)=2CO2(g) ΔH1=-566kJmol-1;S(l)+O2(g)=SO2(g) ΔH2=-296 kJmol-1,则反应热ΔH=___kJmol-1。
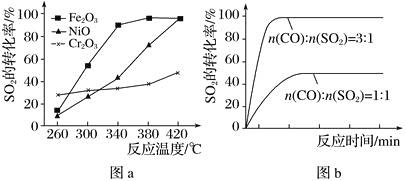
(2)其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图a所示。260℃时___(填“Fe2O3”、“NiO”或“Cr2O3”)作催化剂反应速率最快。Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑价格因素,选择Fe2O3的主要优点是___。
(3)科研小组在380℃、Fe2O3作催化剂时,研究了不同投料比[n(CO):n(SO2)]对SO2转化率的影响,结果如图b所示。请分析当n(CO):n(SO2)=1:1时,SO2转化率接近50%的原因___。
(4)工业上还可用Na2SO3溶液吸收烟气中的SO2:Na2SO3+SO2+H2O=2NaHSO3。某温度下用1.0molL-1Na2SO3溶液吸收纯净的SO2,当溶液中c(SO32-)降至0.2molL-1时,吸收能力显著下降,应更换吸收剂。此时溶液中c(HSO3-)约为___molL-1,溶液的pH=___。(已知该温度下亚硫酸的平衡常数Ka1=1.75×10-2,Ka2=1.25×10-7)
(5)用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如图所示。请写出该电解过程中,阴极区发生反应的方程式:___。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,有机产物只有一种的是
A.乙醇与氧气在铜催化下的氧化反应
B.丙烯(CH3CH=CH2)与HBr的加成反应
C.甲苯在一定条件下发生硝化生成一硝基甲苯的反应
D.异戊二烯(![]() )与等物质的量的Br2发生加成反应
)与等物质的量的Br2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学环分解氯化铵的纯碱和氯乙烯集成清洁工艺如下:

(1)“释氨反应”步骤可能发生的化学反应:
NH4Cl(s)≒ NH3(g)+HCl(g) ΔH=163.57 kJ/mol
MgO(s)+ HCl(g) ≒ MgOHCl(s) ΔH=-102.23 kJ/mol
则总反应NH4Cl(s)+MgO(s)≒NH3(g)+MgOHCl(s) ΔH=____kJ/mol
(2)“释氯反应”可能的化学反应有:
i. MgOHCl(s)≒MgO(s)+ HCl(g) ΔH=+97.50 kJ/mol
ii. MgOHCl(s)+ HCl(g)≒MgCl2(s)+H2O(g) ΔH=+2.89 kJ/mol
iii. MgCl2(s)+ H2O(g)=MgO(s)+2HCl(g) ΔH=+94.61 kJ/mol
图为“释氯反应”在不同温度下各组分的平衡组成,回答下列问题
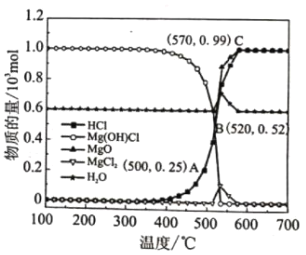
①应选择的最佳反应温度是___________
②500°C时,释氯反应器的压强为P,计算该温度下反应i的平衡常数Kp=___________ (Kp为以分压表示的平衡常数)
③结合平衡移动原理,原料气增加水蒸气的目的是___________
(3)“氯乙烯反应”中,![]() (g)+HCl(g)
(g)+HCl(g)![]() CH2=CHCl(g)的反应机理如图,其中吸附在催化剂表面的物种用*标注
CH2=CHCl(g)的反应机理如图,其中吸附在催化剂表面的物种用*标注
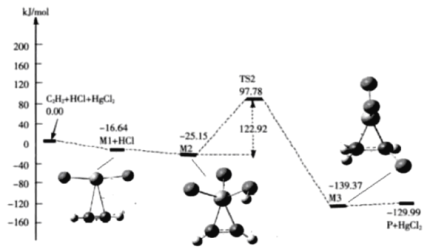
①碳碳叁键的键能:M1_____ ![]() (填“>”或“<”)
(填“>”或“<”)
②“M2→M3”的化学方程式为__________
③该反应的决速步骤为__________
(4)下列有关该工艺的说法不正确的是______(填标号)
A.可循环利用的物质有NH3、MgO、HCl
B.“石灰窑”和“纯碱反应”的副产物可实现资源化利用
C.利用MgO作为吸附剂可有效实现NH3与HCl分离
D.减少了从氯碱工业的产品获取HCl的电能消耗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关.
(1)下列生活用品中,其主要材料属于天然纤维的是_________(填字母序号);
A.塑料保鲜薄 B.橡胶手套 C.棉布围裙
(2)我们常用的洗涤剂清洗餐具上的油污,这是因为洗涤剂具有_________的功能;
(3)食用水果、蔬菜主要补充人体所需的_________;
(4)国家禁止在面粉中添加增白剂过氧化钙CaO2,过氧化钙中氧元素的化合价为_______;
(5)农业上降低土壤酸性的是_________(填化学式);
(6)生活中要用到大量的钢铁,写出赤铁矿(主要成分Fe2O3)冶炼成铁的化学方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等离子
等离子![]() 当向该溶液中逐滴加入一定物质的量浓度的盐酸时,发现生成沉淀的物质的量随盐酸溶液的体积变化的图像如图所示,下列说法正确的是
当向该溶液中逐滴加入一定物质的量浓度的盐酸时,发现生成沉淀的物质的量随盐酸溶液的体积变化的图像如图所示,下列说法正确的是![]()
![]()
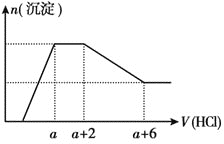
A.原溶液中一定含有![]()
B.反应后最终溶液中的溶质只有![]()
C.原溶液中含有![]() 与
与![]() 的物质的量之比为
的物质的量之比为![]()
D.原溶液中一定含有的阴离子是![]() 、
、![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.增大反应物浓度,可以增大单位体积的活化分子的百分数,使有效碰撞次数增大,反应速率加快
B.H2O2(l)=== ![]() O2(g)+H2O(l) △H=-98 kJ·mol-1,该反应在任何温度下均能自发进行
O2(g)+H2O(l) △H=-98 kJ·mol-1,该反应在任何温度下均能自发进行
C.有气体参加的反应,通入惰性气体,压强增大,从而反应速率加快
D.催化剂不影响反应的活化能,但能增大单位体积的活化分子百分数,加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤气化的一种方法是在气化炉中给煤炭加氢,发生的主要反应为 C(s)+2H2(g) ![]() CH4(g)。在VL 的容器中投入 amol 碳(足量),同时通入 2amolH2,控制条件使其发生上述反应,实验测得碳的平衡转化率随压强及温度的变化关系如图所示。下列说法正确的是( )
CH4(g)。在VL 的容器中投入 amol 碳(足量),同时通入 2amolH2,控制条件使其发生上述反应,实验测得碳的平衡转化率随压强及温度的变化关系如图所示。下列说法正确的是( )
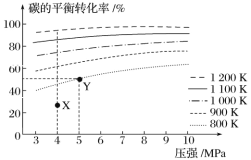
A.在 4MPa、1200K 时,图中 X 点 v 正(H2)<v 逆(H2)
B.在 5MPa、800K 时,该反应的平衡常数为![]()
C.上述正反应为吸热反应
D.工业上维持 6MPa、1000K 而不采用 10MPa、1000K,主要是因为前者碳的转化率高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反应3A(g)+2B(g) ![]() 4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是( )
4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是( )
A. 该反应的化学平衡常数表达式是![]()
B. 此时,B的平衡转化率是40%
C. 增大该体系的压强,化学平衡常数增大
D. 增加B,B的平衡转化率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com