
分析 (1)先根据尾气中二氧化氮和一氧化氮的关系计算二氧化氮、一氧化氮的物质的量,再根据方程式计算氨气和氧气的物质的量,最后根据M=$\frac{m}{n}$计算其平均相对分子质量;(2)根据m=nM计算;
(3)根据V=nVm计算需要氨氧混合气体的体积;
(4)①C=$\frac{1000ρw}{M}$,根据原子守恒知,氮氧化物的物质的量等于氢氧化钠的物质的量,再根据V=$\frac{n}{c}$计算;
②根据方程式2NO2+2NaOH=NaNO2+NaNO3+H2O和NO+NO2+2NaOH=2NaNO2+H2O中氮原子守恒计算NO和NO2的物质的量分别是多少,根据氧原子守恒解答.
解答 解:(1)①设1m3尾气中NO2的物质的量为x,则NO的物质的量为4x,4xmol×30g/mol+46xg=2.49g,x=0.015mol,所以1m3尾气中NO2的物质的量为0.015mol,则NO的物质的量为0.06mol,
根据4NO+4NH3+O2$→_{140℃}^{催化剂}$4N2+6H2O知,0.06molNO需要0.06molNH3,0.015molO2,根据方程式6NO2+8NH3$→_{140℃}^{催化剂}$7N2+12H2O,0.015molNO2需要0.02molNH3,所以氮氧化物混合气体的平均摩尔质量为$\frac{0.015mol×46g/mol+0.06mol×30g/mol}{0.075mol}$=33.2g/mol,所以其相对分子质量为33.2,故答案为:33.2;
(2)1m3尾气中NO的物质的量为0.06mol,所以其m=nM=0.06mol×30g/mol=1800mg,故答案为:1800;
(3)处理1m3尾气需要氨氧混合物的体积=(0.06+0.02+0.015)mol×22.4L/mol=2.128L,则要处理5m3的尾气,需要氨氧混合气的体积为=2.128L×5=10.64L,
故答案为:10.64L;
(3)①C=$\frac{1000×1.28×25%}{40}$,根据原子守恒知,氮氧化物的物质的量等于氢氧化钠的物质的量,所以V=$\frac{0.5mol}{8mol/L}$=62.5mL,故答案为:8;62.5;
②2NO2+2NaOH=NaNO2+NaNO3+H2O和NO+NO2+2NaOH=2NaNO2+H2O,根据氮原子守恒知,生成0.35mol亚硝酸钠则生成0.15mol硝酸钠,生成0.15mol硝酸钠需要0.3mol二氧化氮,同时生成0.15mol亚硝酸钠,0.2mol亚硝酸钠需要0.1mol一氧化氮,所以二氧化氮的物质的量是0.4mol,根据氧原子守恒得x=$\frac{0.1×1+0.4×2}{0.5}$=1.8,
答:x为1.8.
点评 本题考查氧化还原反应及计算,为高频考点,把握反应中物质的量关系、物质的量的基本计算公式为解答的关键,侧重分析与计算能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O CO2 | ||
| C. | CaCl2 NaOH H2O | D. | NH3 H2O CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe(OH)3胶体无色、透明,能发生丁达尔现象 | |
| B. | 水泥厂、冶金厂常用高压电除去烟尘,是因为烟尘微粒带电荷 | |
| C. | 胶体与其它分散系的本质区别是胶体有丁达尔效应,而其它分散系却没有 | |
| D. | 纳米材料 微粒直径从几纳米到几十纳米(1nm=10-9m),因此纳米材料属于胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃放烟花爆竹 | B. | 为城市主干道洒水保洁 | ||
| C. | 大面积开发土建项目 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素非金属性由强到弱的顺序是:Z>Y>X | |
| B. | Y元素最高价氧化物对应水化物的化学式可表示为H4YO4 | |
| C. | 3种元素的气态氢化物中,Z的气态氢化物最稳定 | |
| D. | 原子半径由大到小的顺序为 Z>Y>X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.45mol | B. | 0.8mol | C. | 0.6mol | D. | 0.4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
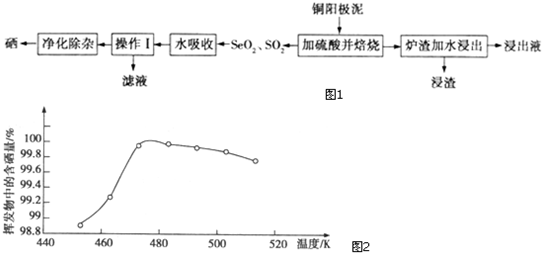
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数K1 | 1.8×10-5 | 4.3×10-7 | 3.0×10-8 |
| K2 | -- | 5.6×10-11 | -- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
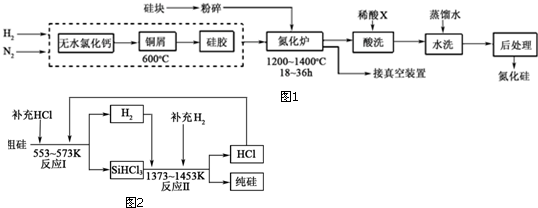
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com