
| A. | 乙烯通入KMnO4溶液中 | B. | 乙烯通入溴水中 | ||
| C. | 甲烷和氯气混合光照 | D. | 苯与浓硫酸、浓硝酸混合加热 |
分析 根据加成反应是有机物分子中的不饱和键发生断裂,不饱和原子直接与其它原子或原子团相结合,生成新的化合物的反应.
解答 解:A.乙烯使KMnO4溶液褪色,是高锰酸钾和乙烯发生了氧化反应的结果,故A错误;
B.乙烯中碳碳双键断裂,分别结合1个溴原子,生成1,2-二溴乙烷,属于加成反应,故B正确;
C.甲烷和氯气混合,光照,甲烷中的氢原子被氯原子代替,生成CH3Cl等氯代甲烷,属于取代反应,故C错误;
D.苯和浓硝酸在浓硫酸作催化剂下反应,苯中的氢原子被硝基代替,生成硝基苯,属于取代反应,故D错误;
故选B.
点评 本题考查学生有机化学中的反应类型,注意各反应类型的特征是解题的关键所在,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 3.5mol•L-1 | B. | 7.0mol•L-1 | C. | 4.5mol•L-1 | D. | 9.0mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
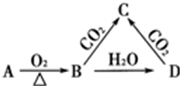
| A. | 与足量盐酸反应放出气体 | B. | 与澄清石灰水反应产生白色沉淀 | ||
| C. | 与氯化钙溶液不反应 | D. | 溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁制管道涂铝粉可防锈蚀 | |
| B. | 碳酸钡、碳酸氢钠、氢氧化镁等均可作为抗酸药物使用 | |
| C. | 焊锡中加铅的目的是提高熔点 | |
| D. | 用废旧皮革生产药用胶囊可以提高原料利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Bi3Ge3O15 | B. | Bi3Ge3O12 | C. | Bi4Ge3O16 | D. | Bi4Ge3O12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X 的能量一定高于M | |
| B. | Y 的能量一定高于N | |
| C. | X 和Y 的总能量一定高于M 和N 的总能量 | |
| D. | 因该反应为放热反应,故不必加热就可发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L H2O含有的分子数为1NA | |
| B. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02NA | |
| C. | 常温常压下,22.4L CO2气体含有原子数为3NA | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 n/mol T/℃ | 活性炭 | NO | E | F |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
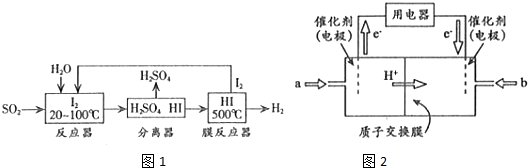
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com