
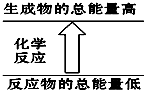
| A. | 铝片与盐酸的反应 | B. | 消石灰与NH4Cl晶体的反应 | ||
| C. | 酸碱中和反应 | D. | 甲烷在氧气中的燃烧反应 |
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M的相对原子质量为32 | B. | M的相对原子质量为64 | ||
| C. | 电解过程中溶液的pH不发生变化 | D. | 电路中通过0.05mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 298K时,CaSO4的溶解度约为7.00×10-2mol/L | |
| B. | 反应CaSO4(s)+CO32-=CaCO3(s)+SO42-在298K时的平衡常数K=Ksp(CaSO4)/Ksp(CaCO3)=1.75×104 | |
| C. | CaCO3、CaSO4的饱和溶液的导电能力很弱,所以它们都是弱电解质 | |
| D. | 升高温度,两种盐的溶度积与溶解度都保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热的纯碱比冷的纯碱去污能力强 | |
| B. | 红棕色NO2加压后颜色先变深后变浅 | |
| C. | SO2催化氧化成SO3的反应,往往需要过量的O2 | |
| D. | H2、I2、HI平衡混和气加压后颜色变深 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com