
O3能吸附有害紫外线,保护人类赖以生存的空间。O3分子的结构如下图所示:呈V形,键角116.5°。三个O原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键:中间O原子提供2个电子,旁边两个O原子分别各提供1个电子,构成一个特殊的化学键——三个O原子均等地享有这4个电子。请回答:
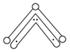
(1)题中非极性共价键是________键,特殊的化学键是________键(填“σ”或“π”)。
(2)1919年,Langmuir提出等电子体的概念:由短周期元素组成的粒子,只要其原子数相等,各原子外层电子数之和相等,也可互称为等电子体。等电子体的结构相似,物理性质相近,根据等电子原理:下列物质的分子与O3分子的结构最相似的是________(填字母)。
A.H2O B.CO2
C.SO2 D.BeCl2
(3)原子中没有跟其他原子共用的电子对叫孤电子对,那么O3分子有________对孤电子对。
(4)下列有关说法中正确的是________(填字母)。
A.臭氧和氧气互为同素异形体,它们在水中的溶解度相近
B.臭氧和氧气的相互转化能保持大气中臭氧的含量基本稳定
C.臭氧转化为氧气和氧气转化为臭氧均需要吸收能量
D.向大气中排放氮的氧化物和氟氯代烃均能加快臭氧的分解
★ ★★
某催化剂中含有的活性组分为Ni、Cu和Zn的化合物,可用于二氧化碳加氢制取甲醚。甲醚是乙醇的同分异构体,其熔点为-141.5 ℃,沸点为-24.9 ℃,在加热条件下可分解成甲烷、乙烷、甲醛等。
(1)乙醇的沸点比甲醚高,其主要原因是_____________________________________。
(2)甲醛分子中碳原子轨道的杂化类型为____________________________________________。
(3)储氢材料化合物A是乙烷的等电子体,其相对分子质量为30.8,且A是由第二周期两种氢化物形成的化合物。加热A会缓慢释放氢气,同时A转化为化合物B,B是乙烯的等电子体。化合物A的结构式为______________(若含有配位键,要求用箭头表示),1 mol化合物B中σ键的数目是________________。
★ ★★


科目:高中化学 来源: 题型:
三氯化氮(NCl3)在常温下是一种淡黄色液体,其分子结构呈三角锥形。则下列说法正确的是( )
A.分子中N—Cl键是非极性键
B.分子中不存在孤对电子
C.它的沸点比PCl3的低
D.因N—Cl键能大,所以NCl3沸点高
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质性质的变化规律,与共价键键能大小有关的是( )
A.F2、Cl2、Br2、I2的熔点、沸点逐渐升高
B.HF、HCl、HBr、HI的热稳定性依次减弱
C.H2O熔沸点高于H2S,HF熔沸点高于HCl
D.NaF、NaCl、NaBr、NaI的熔点依次降低
★ ★★
查看答案和解析>>
科目:高中化学 来源: 题型:
答案 A
解析 本题考查氧化还原反应和阿伏加德罗定律及元素化合物知识,意在考查学生利用有关定律进行数据处理的能力。氮氧化合物与铜粉反应生成CuO和N2,结合题中气体体积和阿伏加德罗定律可推知该氮的氧化物分子中只含有一个氮原子,结合选项知A正确。
★ ★★
查看答案和解析>>
科目:高中化学 来源: 题型:
右图的装置中,干燥烧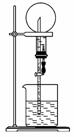 瓶内盛有某种气体,烧杯和滴管内盛放某种溶液。挤压滴管的胶头,下列与实验事实不相符的是( )
瓶内盛有某种气体,烧杯和滴管内盛放某种溶液。挤压滴管的胶头,下列与实验事实不相符的是( )
A.CO2(NaHCO3溶液)/无色喷泉
B.NH3(H2O中含酚酞)/红色喷泉
C.H2S(CuSO4溶液)/黑色喷泉
D.HCl(AgNO3溶液)/白色喷泉
★ ★★
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y、Z三种主族元素在元素周期表中的位置如图所示,设X的原子序数为a。则下列说法不正确的是( )
| Y | ||
| X | ||
| Z |
A.Y与Z的原子序数之和可能为2a
B.Y的原子序数可能为a-17
C.Z的原子序数可能为a+31
D.X、Y、Z一定为短周期元素
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D四种短周期元素的原子半径依次减小,A与C的核电荷数之比为3∶4,D能分别与A、B、C形成电子总数相等的分子X、Y、Z。下列叙述正确的是( )
A.X、Y、Z的稳定性逐渐减弱 B.A、B、C、D只能形成5种单质
C.X、Y、Z三种化合物的熔、沸点逐渐升高 D.自然界中不存在由A、B、C、D四种元素组成的化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com