
| A�� | K2CO3��Һ�У�$\frac{1}{2}$c��K+��=c��CO32-��+c��HCO3-��+c��H2CO3�� | |
| B�� | ijŨ�ȵ�NaAc��Һ��pH=8�������Һ�е�c��Na+��-c��Ac-��=9.9��10-7mol/L | |
| C�� | ���ʵ���Ũ����ȵĢ�NH4Cl���ڣ�NH4��2SO4������Һ��c��NH4+����С˳��Ϊ���٣��� | |
| D�� | 10mLpH=12���ռ���Һ�м���pH=2����HA�����ԣ���������Һ�����V��10mL |
���� A���κε������Һ�ж�����ԭ���غ㣬����ԭ���غ��жϣ�
B��ijŨ�ȵ�NaAc��Һ��pH=8����NaAcΪǿ�������Σ���Һ��c��H+��=10-8mol/L��c��OH-��=10-6mol/L����Һ��c��Na+��-c��Ac-��=c��OH-��-c��H+����
C����������ζ���ǿ�������Σ�笠�����ˮ��̶���ͬ��
D��pH=12��NaOH��Һ��c��NaOH��=0.01mol/L��pH=2��HA��Һ��c��HA����0.01mol/L��Ҫʹ�����Һ�����ԣ������ǿ�ᣬ���������ʵ�����ȣ���������ᣬ��������ʵ���Ӧ������Щ��
��� �⣺A���κε������Һ�ж�����ԭ���غ㣬����ԭ���غ��c��K+��=2c��CO32-��+2c��HCO3-��+2c��H2CO3������A����
B��ijŨ�ȵ�NaAc��Һ��pH=8����NaAcΪǿ�������Σ���Һ��c��H+��=10-8mol/L��c��OH-��=10-6mol/L����Һ��c��Na+��-c��Ac-��=c��OH-��-c��H+��=10-6mol/L-10-8mol/L=9.9��10-7mol/L����B��ȷ��
C����������ζ���ǿ�������Σ�笠�����ˮ��̶���ͬ������c��NH4+����С˳��Ϊ���٣��ڣ���C����
D��pH=12��NaOH��Һ��c��NaOH��=0.01mol/L��pH=2��HA��Һ��c��HA����0.01mol/L��Ҫʹ�����Һ�����ԣ������ǿ�ᣬ���������ʵ�����ȣ���������ᣬ��������ʵ���Ӧ������Щ�����������������ǵ���10��mL��Ҳ����С��10mL����D����
��ѡB��
���� ���⿼������Ũ�ȴ�С�Ƚϣ�Ϊ��Ƶ���㣬�漰����ˮ�⡢������ʵĵ����֪ʶ�㣬��ȷ��Һ�����ʳɷּ��������ǽⱾ��ؼ���ע�����غ㡢ԭ���غ��������ã��״�ѡ����B��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��FeCl3��Һ��ʴͭ��·�壺Cu+2Fe3+=Cu2++2Fe2+ | |
| B�� | �������������������Fe3O4+8H+=3Fe3++4H2O | |
| C�� | ������������Һ��ȥ�����������Ĥ��Al2O3+2OH-=2AlO2-+H2O | |
| D�� | �����ۼ���ϡ�����У�2Fe+6H+=2Fe3++3H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
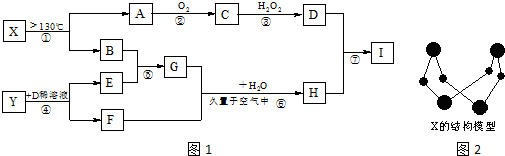
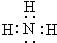 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ӻ������У�һ�������ӿ�ͬʱ����������֮���о������� | |
| B�� | ���ӻ������е������Ӷ��ǽ������� | |
| C�� | ����ˮ���Ե���Ļ�����һ�������ӻ����� | |
| D�� | ���ǽ���Ԫ�ظ��ǽ���Ԫ�ػ��϶��γ����ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
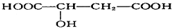 ��ƻ������ܷ����ķ�Ӧ�ǣ�������
��ƻ������ܷ����ķ�Ӧ�ǣ�������| A�� | �٢ڢ� | B�� | �٢ڢۢ� | C�� | �٢ڢۢ� | D�� | �٢ڢۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
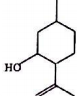
| A�� | �����ʽΪC10H18O | B�� | ����1������̼ԭ�� | ||
| C�� | �ܷ�����ȥ��Ӧ | D�� | ����FeCl3��Һ��Ӧ��ʾ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
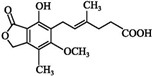
| A�� | ����ʽΪC17H18O6 | B�� | ����������֬�������� | ||
| C�� | ֻ�����ֹ����� | D�� | �����ʿɷ���������Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com