
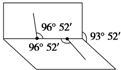
 已知H2O2分子的结构如图所示:H2O2分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角为93°52′,而两个O-H键与O-O键的夹角均为96°52′.
已知H2O2分子的结构如图所示:H2O2分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角为93°52′,而两个O-H键与O-O键的夹角均为96°52′.

科目:高中化学 来源: 题型:
| A、0.6 mol/L |
| B、0.8 mol/L |
| C、1.0 mol/L |
| D、1.2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
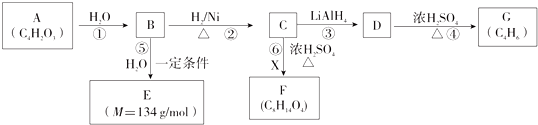

| H2O |
| LiAlH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 A
A| 一定条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓硝酸保存在棕色试剂瓶中 |
| B、金属钠通常保存在煤油里,不能保存在四氯化碳中 |
| C、烧碱溶液保存在带玻璃塞的磨口试剂瓶中 |
| D、配置一定物质的量浓度的氯化钠溶液时,要将氯化钠固体放在滤纸上称量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4、C3H6 |
| B、CH4、C2H4 |
| C、C2H4、C3H8 |
| D、C2H6、C3H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 某溶液W进行焰色反应实验 | 焰色为黄色 | W一定是钠盐溶液 |
| B | 蘸有浓氨水的玻璃棒靠近溶液X | 有白烟产生 | X可能是浓盐酸 |
| C | 强酸性溶液Y中加入Ba(NO3)2溶液,静置后再加入KSCN溶液 | 先有白色沉淀,后溶液又变红 | Y中一定含有SO42-和Fe3+ |
| D | 气态炔烃Z通入pH=α的溴水中 | 溴水褪色,溶液的pH>α | Z与溴发生了取代反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向蒸馏水中滴加浓H2SO4时,KW不变 |
| B、常温下,0.005mol?L-1Ba(OH)2溶液pH为12 |
| C、NaHCO3水解的离子方程式为:HCO3-+H2O?CO32-+H3O+ |
| D、NaHSO3属于强碱弱酸盐,其水溶液一定显碱性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com