
【题目】能证明乙醇的分子组成为CH3CH2OH,而不是CH3OCH3,最充分的理由是 ( )
A. 1 mol乙醇与足量钠反应放出0.5 mol氢气
B. 1 mol乙醇完全燃烧需要3 mol氧气
C. 1 mol生成2 mol二氧化碳和3 mol水
D. 4.6 g乙醇在标准状况下的体积为2.24 L
 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】下列反应中,属于放热的氧化还原反应的是 ( )
A.Ba(OH)2·8H2O与NH4Cl反应B.生石灰和水的反应
C.甲烷与O2的燃烧反应D.灼热的炭与CO2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O的反应中,被还原的硝酸的物质的量与未被还原的硝酸的物质的量之比为( )
A.1:2B.1:3C.3:1D.1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是( )
A. 向0.1 mol·L-1 CH3COOH溶液中加入少量水,溶液中![]() 减小
减小
B. 将CH3COONa溶液从20 ℃升温至30 ℃,溶液中![]() 增大
增大
C. 在pH=8的NaB溶液中:c(Na+)﹣c(B﹣)=9.9×10﹣8mol![]() L﹣1
L﹣1
D. 向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中![]() 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知(CH3COOH)2(g)![]() 2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量随温度(T)的变化曲线如图所示,下列说法正确的是( )
2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量随温度(T)的变化曲线如图所示,下列说法正确的是( )
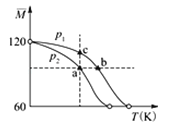
A. 该过程的△H<0
B. 气体压强:p(a)<p(b)= p(c)
C. 平衡常数:K(a)= K(b)< K(c)
D. 测定乙酸的相对分子质量要在高压、低温条件
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是形成化合物种类最多的元素,其单质及化合物有独特的性质和用途。请回答下列问题。
(1)碳原子核外电子有_____种不同的运动状态。碳原子的价电子在形成sp3杂化后,其轨道表达式为_____。
(2)写出一种CO32-的等电子体微粒的化学式_______,其空间构型为_______。
(3)有机物M(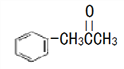 )在一定条件下生成N(
)在一定条件下生成N( )。
)。
①沸点:M_____N (填“大于”或“小于”)。
②M中碳原子杂化类型为_____,不同杂化类型的碳原子数之比为_____。
③有机物N中除氢原子之外的其他原子的第一电离能由大到小的顺序为_____。
(4)已知CaCO3的热分解温度为900℃,SrCO3的热分解温度为1172℃,试从原子结构的角度解释CaCO3的热分解温度低于SrCO3的原因_____________。
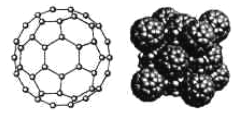
(5)碳的一种同素异形体C60,又名足球烯,是一种高度堆成的球碳分子。立方烷(分子式:C8H8,![]() )是比C60约早20年合成出的一种对称性烃类分子,而如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原C60晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为______________。
)是比C60约早20年合成出的一种对称性烃类分子,而如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原C60晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为______________。
(6)石墨是碳的一种同素异形体,它的一种晶胞结构和部分晶胞参数如下图:
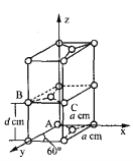
①原子坐标参数描述的是晶胞内原子间的相对位置。石墨晶胞中碳原子A、B的坐标参数分别为:A(0,0,0)、B(0,1,1/2)。则C原子的坐标参数为_______________。
②晶胞参数用以描述晶胞的大小和形状。已知石墨晶胞底边长为acm ,层间距为dcm,阿伏加德罗常数的值为NA,则石墨的密度为_____g·cm-3(写出表达式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度下,将2molA和3molB充入一密闭容器中,发生反应:aA(g)+B(g) ![]() C(g)+D(g),5min后达到平衡,各物质的平衡浓度的关系为:ca(A)c(B)=c(C)c(D)。若在温度不变的情况下将容器的体积扩大为原来的8倍,A的转化率不发生变化,则B的转化率为( )
C(g)+D(g),5min后达到平衡,各物质的平衡浓度的关系为:ca(A)c(B)=c(C)c(D)。若在温度不变的情况下将容器的体积扩大为原来的8倍,A的转化率不发生变化,则B的转化率为( )
A. 60% B. 40% C. 50% D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列操作中,所使用的仪器能够达到目的是( )
A.用5mL量筒准确量取4.55mL水
B.称量4.5g纯碱时,将纯碱放在称量纸上置于托盘天平的右盘,将砝码放在托盘天平的左盘
C.过滤时用玻璃棒搅拌漏斗内的液体,以加速过滤
D.萃取操作时,选择萃取剂的密度可以比水大也可以比水小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某次实验需用480mL、0.5mol/L的稀H2SO4溶液,某同学用98%的浓H2SO4(ρ=1.84g/cm3)进行配制,请回答下列问题:
(1)实验需要的玻璃仪器除了烧杯、量筒、玻璃棒,还有________________________;
(2)计算:98%的浓H2SO4(ρ=1.84g/cm3)的物质的量浓度为__________,配制本次实验需要的稀硫酸需用量筒量取上述98%的浓H2SO4___________________ mL
(3)配制过程:①用量筒量取所需的浓硫酸
②将浓硫酸缓缓注入盛有适量蒸馏水的烧杯中,边加边搅拌
③用玻璃棒引流将烧杯中的溶液转移到已经检漏的合适规格的容量瓶中
④洗涤烧杯和玻璃棒2~3次,洗涤液也注入容量瓶中.轻轻摇动容量瓶,使溶液混合均匀
⑤向容量瓶中加入蒸馏水,在距离刻度1~2cm时,改用胶头滴管加蒸馏水至刻度线
⑥盖好瓶塞,反复上下颠倒,摇匀
⑦将配制好的溶液转移至试剂瓶中待用。
上述配置溶液的步骤存在缺失,缺少的步骤是_____________________,应放在步骤_____之前进行(填“序号”)。
(4)在横线上填写下列各种情况对所配制溶液浓度的影响(选填“偏高”、“偏低”或“无影响”).
①所用的浓硫酸长时间放置在密封不好的容器中_________;
②量取浓硫酸所用量筒有蒸馏水_________;
③定容时,俯视液面_________;
④用量筒量取浓硫酸时仰视液面___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com