
NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如下:
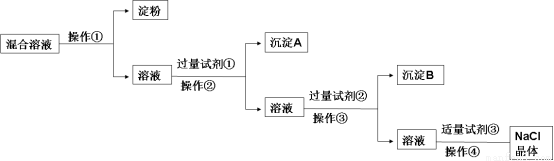
(1)写出上述实验过程中所用试剂(写化学式):
试剂①_______________________;试剂③________________________。
(2)判断试剂①已过量的方法是:________________________________________。
(3)用化学方程式表示加入试剂②的作用:
(4)操作①是利用半透膜进行分离提纯。
操作①的实验结果:淀粉 (填“能”或“不能”)透过半透膜;
SO42- (填“能”或“不能”)透过半透膜;
请用实验证明上述结果,完成下表(可不填满,也可增加):
限选试剂:1mol/L AgNO3溶液、1mol/L BaCl2溶液、1mol/L Ba(NO3)2溶液、
碘水、稀盐酸、稀硝酸
编号 | 实验操作 | 预期现象和结论 |
① |
|
|
② |
|
|
|
|
|
(1)BaCl2(2分);HCl(2分)(2)静置,向上层清液中滴加少量氯化钡溶液,没有白色沉淀产生,说明氯化钡溶液已过量。(2分)
(3)BaCl2+Na2CO3=2NaCl+BaCO3↓ CaCl2+Na2CO3=2NaCl+CaCO3↓(每方程式2分,共4分))
(4)不能(1分); 能(1分); 填表(共8分)
编号 | 实验操作 | 预期现象和结论 |
① | 取半透膜外液体,加入少量碘水(2分) | 液体没有变成蓝色,证明淀粉不能透过半透膜(2分) |
② | 另取半透膜外液体,加入足量稀盐酸和少量1mol/L BaCl2溶液(2分) | 产生不溶于盐酸的白色沉淀,证明SO42-能够透过半透膜(2分) |
【解析】
试题分析:根据题给流程图分析:混合液先通过渗析分离出淀粉胶体,再向剩余溶液中加过量氯化钡溶液, 除去硫酸根,然后再加过量的碳酸钠溶液除去钙离子和过量的钡离子,过滤后向滤液中加适量盐酸,除去过量的碳酸钠,蒸发的氯化钠晶体。(1)根据上述分析知,试剂①为BaCl2;试剂③HCl。(2)判断氯化钡溶液已过量的方法是:静置,向上层清液中滴加少量氯化钡溶液,没有白色沉淀产生,说明氯化钡溶液已过量。(3)加过量的碳酸钠溶液目的是除去钙离子和过量的钡离子,反应的化学方程式为 BaCl2+Na2CO3=2NaCl+BaCO3↓ CaCl2+Na2CO3=2NaCl+CaCO3↓。(4)利用溶液中小的分子或离子能透过半透膜,胶体微粒不能透过半透膜,采用渗析的方法将二者分离,然后再分别用碘单质检验淀粉,用盐酸和氯化钡溶液检验硫酸根;实验方案见答案。
考点:考查物质的分离和提纯的基本操作。


科目:高中化学 来源:2016届江苏省东台市高一上学期期末考试化学试卷(解析版) 题型:选择题
石棉是硅酸盐矿物,某种石棉的化学式表示为: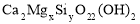 ,该化学式中x, y的值分别是( )
,该化学式中x, y的值分别是( )
A.5、8 B.8、3 C.3、8 D.8、5
查看答案和解析>>
科目:高中化学 来源:2016届广东省高一上学期期中考试化学试卷(解析版) 题型:选择题
仅用下表提供的玻璃仪器(非玻璃仪器任选)或实验装置(图1、图2)就能实现相应实验目的是( )
选项ABCD
实验项目除去KCl中少量的MnO2用10mol/L的盐酸配制100mL0.1mol/L的盐酸用氯化钠溶液制备氯化钠晶体 除去CO2气体中的HCl
实验仪器
或装置烧杯、玻璃棒、漏斗100mL容量瓶、玻璃棒、烧杯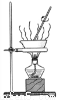
图1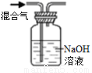
图2
查看答案和解析>>
科目:高中化学 来源:2016届广东省梅州市高一上学期质检化学试卷(解析版) 题型:填空题
用Na2CO3固体配制1mol/L的Na2CO3溶液100mL。
(1)供选用的仪器有:①玻璃棒;②胶头滴管;③100mL量筒;④100mL容量瓶;⑤250mL量筒;⑥天平;⑦50mL烧杯;应选用的仪器(填编号) 。
(2)应称取Na2CO3的质量为
(3)有三瓶标签脱落的无色透明溶液,分别是稀盐酸、稀硫酸和稀硝酸。请你帮助实验老师设计两种方法鉴别它们,并贴上标签。
| 操 作 步 骤 | 现 象 及 结 论 |
方法一 |
|
|
方法二 |
|
|
查看答案和解析>>
科目:高中化学 来源:2016届广东省梅州市高一上学期质检化学试卷(解析版) 题型:选择题
下列各组中的离子,能在溶液中大量共存的是( )
A.H+ Na+ CO32- Cl- B.Ba2+ Na+ Cl- SO42-
C.K+ H+ SO42- OH- D.Ag+ Al3+ NO3- H+
查看答案和解析>>
科目:高中化学 来源:2016届广东省高一上学期期中考试化学试卷(解析版) 题型:选择题
溶液、胶体和浊液这三种分散系的根本区别是
A.是否是大量分子或离子的集合体 B.分散质粒子直径的大小
C.是否能通过滤纸或半透膜 D.是否均一、稳定、透明
查看答案和解析>>
科目:高中化学 来源:2016届广东省佛山市质量检测化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.碳酸氢钠与稀盐酸反应:HCO3—+H+=CO2↑+H2O
B.铝溶于NaOH溶液:Al+2OH—=AlO2—+H2↑
C.碳酸镁中滴加稀盐酸:CO32—+2H+=CO2↑+H2O
D.硫酸铜溶液中滴加氢氧化钡溶液:Cu2++2OH—=Cu(OH)2↓
查看答案和解析>>
科目:高中化学 来源:2016届山西省朔州市高一上学期第四次月考化学试卷(解析版) 题型:选择题
将0.1 mol的MnO2和40 mL 10 mol·L-1的浓盐酸混合后加热,充分反应后,向所得溶液中加入足量的AgNO3溶液。在此过程中:
(1)产生的Cl2在标准状况下的体积V(Cl2)为______(填写体积范围);
(2)产生的AgCl沉淀的物质的量为______ (假设盐酸不挥发,且产生的Cl2的物质的量为a mol)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com