
【题目】分枝酸可用于生化研究。其结构简式如下图。下列关于分枝酸的叙述正确的是( )
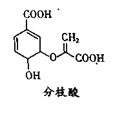
A.分子中含有3种官能团
B.1mol分枝酸最多可与3mol NaOH发生中和反应
C.可与乙醇、乙酸反应,且反应类型相同
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】H2C2O4为二元弱酸。20℃时,配制一组c(H2C2O4)+ c(HC2O4-)+ c(C2O42-)="0.100" mol·L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如右图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是

A. pH=2.5的溶液中:c(H2C2O4)+ c(C2O42-)> c(HC2O4-)
B. c(Na+)="0.100" mol·L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+ c(C2O42-)
C. c(HC2O4-)= c(C2O42-)的溶液中:c(Na+)>0.100 mol·L-1+ c(HC2O4-)
D. pH=7的溶液中:c(Na+)>2c(C2O42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】那可丁是一种药物,该药物适用于刺激性干咳病人服用,无成瘾性,化合物H是制备该药物的重要中间体,合成路线如下:
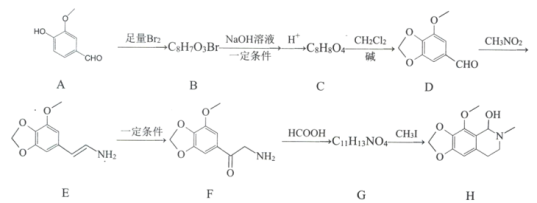
已知:①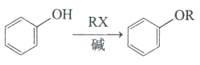
②RNH2 ![]() RNHCH3
RNHCH3
(1)化合物B的结构简式:________。
(2)反应B→C的第一步反应类型:____________。
(3)下列说法正确的是:___________。
A 物质D能与FeCl3发生显色反应 B 物质F具有碱性
C 物质G能和银氨溶液发生反应 D 物质H的分子式是C12H15NO4
(4)写出C→D的化学方程式:____________。
(5)请写出化合物H满足下列条件的所有同分异构体的结枸简式:_______________。
①分子中含苯环,无其他环状结构
②分子中含有NO2且直接连在苯环上
③分子中只有3种不同化学环境的氢
(6)已知CH2=CHCH3![]() CH2CHCH2Cl,请以
CH2CHCH2Cl,请以![]() 、CH3CHClCH3为原料合成化合物
、CH3CHClCH3为原料合成化合物![]() ,写出制备的合成路线流程图(无机试剂任选)______________。
,写出制备的合成路线流程图(无机试剂任选)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:常温下,![]()
![]() ,
,![]() ,某二元酸
,某二元酸![]() 及其钠盐的溶液中,
及其钠盐的溶液中,![]() 、
、![]() 、
、![]() 分别在三者所占的物质的量分数
分别在三者所占的物质的量分数![]() 随溶液pH变化关系如图所示,下列叙述错误的是
随溶液pH变化关系如图所示,下列叙述错误的是

A.在![]() 的溶液中:
的溶液中:![]()
B.等体积等浓度的NaOH溶液与![]() 溶液混合后,溶液中水的电离程度比纯水小
溶液混合后,溶液中水的电离程度比纯水小
C.在![]() 的溶液中存在
的溶液中存在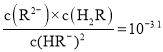
D.向![]() 溶液中加入少量
溶液中加入少量![]() 溶液,发生反应:
溶液,发生反应:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.油脂皂化反应得到高级脂肪酸盐与甘油
B.在一定条件下,苯与液溴、硝酸、硫酸作用生成溴苯、硝基苯、苯磺酸的反应都属于取代反应
C.己烷有4种同分异构体,它们的熔点、沸点各不相同
D.聚合物(![]() )可由CH3CH=CH2和CH2=CH2加聚制得
)可由CH3CH=CH2和CH2=CH2加聚制得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是易溶于水且不与水反应的黄绿色气体,沸点为11℃。某小组在实验室中制备ClO2的装置如下:[已知:SO2+2NaClO3+H2SO4=2ClO2 +2NaHSO4]

下列说法正确的是
A.装置C中装的是饱和食盐水,a逸出的气体为SO2
B.连接装置时,导管口a应接h或g,导管口c应接e
C.装置D放冰水的目的是液化SO2,防止污染环境
D.可选用装置A利用1mol·L1盐酸与MnO2反应制备Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾(FeSO4·7H2O)外观为半透明蓝绿色单斜结晶或颗粒,无气味。受热能分解,且在空气中易被氧化。
I.医学上绿矾可用于补血剂甘氨酸亚铁[(NH2CH2COO)2Fe]颗粒的制备,有关物质性质如下:
甘氨酸(NH2CH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
易溶于水,微溶于乙醇,两性化合物 | 易溶于水和乙醇,有强酸性和还原性 | 易溶于水,难溶于乙醇 |
(1)向绿矾溶液中,缓慢加入NH4HCO3溶液,边加边搅拌,反应结束后生成沉淀FeCO3。该反应的离子方程式为_______。
(2)制备(NH2CH2COO)2Fe:往FeCO3中加入甘氨酸(NH2CH2COOH)的水溶液,滴入柠檬酸溶液并加热。反应结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥得到产品。
①加入柠檬酸溶液一方面可调节溶液的pH促进FeCO3溶解,另一个作用是__。
②洗涤操作,选用的最佳洗涤试剂是_______(填序号)。
A.热水 B.乙醇 C.柠檬酸
II.绿矾晶体受热分解的反应为2FeSO4·7H2O![]() Fe2O3+SO2↑+SO3↑+14H2O,实验室用图I所示装置验证其分解产物。请回答下列问题:
Fe2O3+SO2↑+SO3↑+14H2O,实验室用图I所示装置验证其分解产物。请回答下列问题:
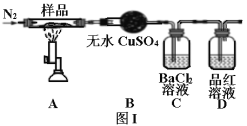
(1)加热前通入氮气的目的是_______。
(2)实验中观察到装置B现象为_______。
(3)C装置和D装置能否调换_______(填“能”或“否”)。
(4)样品完全分解后,残留物全部为红棕色固体,检验装置A中的残留物含有Fe2O3的方法是_______。
(5)该装置有个明显缺陷是_______。
III.测定绿矾样品中铁元素的含量。
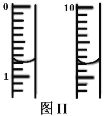
称取m g绿矾样品于锥形瓶中溶解后加稀H2SO4酸化,用 c mol·L1 KMnO4 溶液滴定至终点。耗KMnO4溶液体积如图II所示,(滴定时发生反应的离子方程式为:5Fe2++MnO4+8H+=5Fe3++Mn2++4H2O),该晶体中铁元素的质量分数为_______(用含m、c的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000![]() NaOH溶液滴定20.00mL某未知浓度的CH3COOH溶液,滴定曲线如右图所示。已知在点③处恰好中和。下列说法不正确的是( )
NaOH溶液滴定20.00mL某未知浓度的CH3COOH溶液,滴定曲线如右图所示。已知在点③处恰好中和。下列说法不正确的是( )

A. 点①②③三处溶液中水的电离程度依次增大
B. 该温度时CH3COOH的电离平衡常数约为![]()
C. 点①③处溶液中均有c(H+)=c(CH3COOH)+c(OH-)
D. 滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.足量的KI溶液与FeCl3溶液反应后,用CCl4萃取其中的I2,分液,在水溶液中滴加KSCN溶液仍呈血红色,说明该反应有一定的限度
B.在一定条件下,一份双氧水样品经过2h,H2O2的浓度从0.05molL-1下降到0.03molL-1,H2O2在这2h中分解的平均反应速率约为0.015molL-1h-1
C.其他条件相同时,升高温度,对于吸热反应,反应速率加快,对于放热反应,反应速率减慢
D.一定条件下,固定体积的密闭容器中发生反应A(g)+B(g)2C(g),当容器内A、B、C的浓度之比为1:1:2时,该反应处于平衡状态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com