
| A、Z是第二周期ⅣA族元素 |
| B、最高价氧化物对应的水化物的酸性:Y<X |
| C、非金属性:X<Y<Z |
| D、X、Y、Z的氢化物稳定性逐渐减弱 |


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CO2+C
| ||||
B、2Na+O2
| ||||
| C、Mg+2HCl═MgCl2+H2↑ | ||||
D、2Al+Fe2O3
|
查看答案和解析>>
科目:高中化学 来源: 题型:
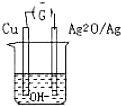 普通水泥在固化过程中自由水分子减少并产生胶体溶液呈碱性.根据这一物理化学特点科学家发明了电动势法测水泥初凝时间.此法的原理如图所示,反应的总方程式为2Cu+Ag2O=Cu2O+Ag 下列有关说法正确的是( )
普通水泥在固化过程中自由水分子减少并产生胶体溶液呈碱性.根据这一物理化学特点科学家发明了电动势法测水泥初凝时间.此法的原理如图所示,反应的总方程式为2Cu+Ag2O=Cu2O+Ag 下列有关说法正确的是( )| A、工业上以黏土、石灰石为主要原料来制造水泥 |
| B、测量原理示意图中 Ag2O为负极 |
| C、负极的电极反应式为:2Cu+2OH--2e-=Cu2O+H2O |
| D、电池工作时OH-向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、18g水中含有的氢原子数为NA |
| B、0.1mol钠离子含有的电子数为NA |
| C、标准状况下,22.4L苯含有的分子数为NA |
| D、1mol/L的氯化钡溶液中,含有的钡离子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA |
| B、由CO和O2组成的混台物中共有NA个分子,其中的氧原子数为2NA |
| C、在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,转移电子数为2NA个 |
| D、0.1mol Fe粉与足量水蒸气反应生成的H2分子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com