
A﹣H分别是中学化学中的常见物质,它们之间有下图所示关系(反应中所需要和所生成的水均没有列出),已知B、H为常见的金属单质,A、C均为气体单质且A气体的颜色为黄绿色,F的水溶液为蓝色,B、D、G、E中均含同一种元素.请回答:
(1)A、B、G、H分别是什么物质?(写物质名称)
A ,B铁,G ,H
(2)写出D→F反应的离子方程式: .
(3)写出G和稀盐酸反应的化学方程式: .
(4)2molB与足量的A完全反应生成D时所转移的电子为 mol.
(5)如何检验D溶液中的阳离子? .

考点: 无机物的推断.
分析: A为气体单质且A气体的颜色为黄绿色,推知A为氯气;F的水溶液为蓝色,可知F为铜盐;B为常见的金属单质,B、D、G、E中均含同一种元素,可知B为一种变价金属,B为铁,D为氯化铁,E为氯化亚铁,则G为四氧化三铁,C为氧气,以此来解答.
解答: 解:A为气体单质且A气体的颜色为黄绿色,推知A为氯气;F的水溶液为蓝色,可知F为铜盐;B为常见的金属单质,B、D、G、E中均含同一种元素,可知B为一种变价金属,B为铁,D为氯化铁,E为氯化亚铁,则G为四氧化三铁,C为氧气,
(1)由上分析A为氯气,B为铁,G为四氧化三铁,H为铜,故答案为:氯气;铁;四氧化三铁;铜;
(2)氯化铁生成铜盐反应离子方程式为2Fe3++Cu=2Fe3++Cu2+,故答案为:2Fe3++Cu=2Fe3++Cu2+;
(3)四氧化三铁与盐酸反应的化学反应方程式为Fe3O4+8HCl=FeCl2+2FeCl3+4H2O,故答案为:Fe3O4+8HCl=FeCl2+2FeCl3+4H2O;
(4)2mol铁与足量的氯气反应生成氯化铁,Fe由0价升高到+3价,1molFe失去3mol电子,2molFe失去6mol电子,故答案为:6;
(5)检验Fe3+的方法是取少量D溶液与试管中,加入KSCN溶液,溶液变为血红色,证明D溶液中的氧离子是Fe3+,故答案为:取少量D溶液与试管中,加入KSCN溶液,溶液变为血红色,证明D溶液中的氧离子是Fe3+.
点评: 本题考查无机物的推断,注意推断的关键点:A、C均为气体单质且A气体的颜色为黄绿色,F的水溶液为蓝色,再结合物质的其它性质分析解答,题目难度较大.


科目:高中化学 来源: 题型:
在溶液中能大量共存,加入OH﹣有沉淀析出,加入H+有气体放出的是()
A. Mg2+、Na+、Cl﹣、CO32﹣ B. Fe3+、K+、SO42﹣、NO3﹣
C. H+、Al3+、OH﹣、NO3﹣ D. Na+、Ca2+、Cl﹣、HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
同周期的X、Y、Z三种元素,已知其高价氧化物对应的水化物的酸性强弱顺序是:HXO4>H2YO4>H3ZO4,则下列各判断中正确的是()
A. 原子半径:X>Y>Z B. 原子序数:X<Y<Z
C. 气态氢化物稳定性:X<Y<Z D. 非金属性:X>Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
不能说明X的电负性比Y的大的是( )
|
| A. | 与H2化合时X单质比Y单质容易 |
|
| B. | X的最高价氧化物的水化物的酸性比Y的最高价氧化物的水化物的酸性强 |
|
| C. | X原子的最外层电子数比Y原子的最外层电子数多 |
|
| D. | X单质可以把Y从其氢化物中置换出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知三角锥形分子E和直线形分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10)如图,则下列判断错误的是( )
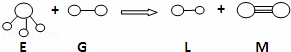
|
| A. | G是电负性最大的元素 |
|
| B. | 1个M分子中有2个σ键 |
|
| C. | E易液化是因为相对分子质量较大 |
|
| D. | L是极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某银白色金属单质A在空气中加热燃烧时发出黄色火焰,得到淡黄色固体B,A露置在空气中足够长时间变为C,B和酸性气体D能生成C,A和B都能与水生成E,E和D也能生成C.回答下列问题.
(1)写出下列物质的化学式:C ,D ,E .
(2)写出下列反应的化学方程式:
①A和水生成E: .
②B和D生成C: .
③Cl2与E的水溶液: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com