
| A. | 0.1 mol NaHSO4晶体中含阴阳离子总数是0.3NA | |
| B. | 将0.1mol FeCl3加到沸水中制得的胶体中,含胶粒0.1NA | |
| C. | 1 mol Na2O2与足量H2O完全反应,转移电子数目为2NA | |
| D. | 在常温常压下,13.8g NO2与足量水充分反应,剩余气体的分子数为0.1NA |
分析 A.硫酸氢钠是由钠离子与硫酸氢根离子构成;
B.一个氢氧化铁胶粒是多个氢氧化铁的聚集体;
C.过氧化钠与水反应为歧化反应;
D.3mol二氧化氮与水反应生成1molNO;
解答 解:A.0.1 mol NaHSO4晶体中含0.1mol钠离子,0.1mol硫酸氢根离子,阴阳离子总数是0.2NA,故A错误;
B.一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故形成的胶粒的个数小于0.1NA个,故B错误;
C.过氧化钠与水反应为歧化反应,1 mol Na2O2与足量H2O完全反应,转移电子数目为NA,故C错误;
D.3mol二氧化氮与水反应生成1molNO,13.8克NO2的物质的量为0.3mol,与足量水充分反应,剩余气体的分子数为0.1NA,故D正确;
故选:D.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.试题有利于培养学生的逻辑推理能力,题目难度不大.


科目:高中化学 来源: 题型:实验题

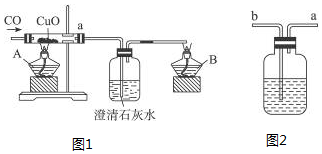
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ①②③ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过量的SO2通入NaOH溶液中:SO2+2OH-═SO32-+H2O | |
| B. | 用醋酸溶解CaCO3:2H+CaCO3═Ca2++H2O+CO2↑ | |
| C. | 在氯化亚铁溶液中通入氯气Fe2++Cl2═Fe3++2Cl- | |
| D. | NaHCO3溶液中加入过量的Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
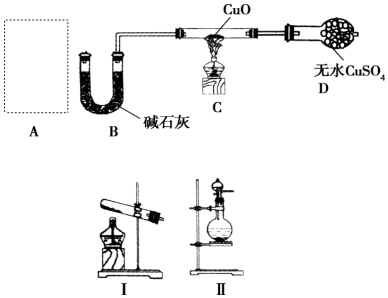
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
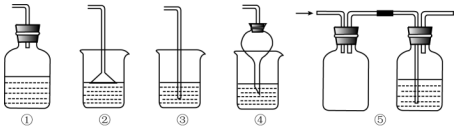
| A. | ②④⑤ | B. | ①②④ | C. | ①②③ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 71gCl2含有的氯原子数目为NAB | |
| B. | 标准状况下,2.24L水所含的分子数为0.1NA | |
| C. | 1mol•L-1AlCl3溶液中含有的Cl-数目为3NA | |
| D. | 2.4g金属镁变成镁离子时失去的电子数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,36 g 18O2中所含的中子数为16 NA | |
| B. | 8.0 g Cu2S和CuO的混合物中含有的铜原子数为0.1 NA | |
| C. | 电解饱和食盐水时,阳极生成22.4L气体时,阴极生成气体分子 NA个 | |
| D. | 标准状况下,22.4 L Cl2与足量NaOH溶液反应,转移电子数为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com