
盐是一类常见物质,下列物质可直接和适当的物质反应生成盐的是
①金属 ②碱性氧化物 ③碱 ④非金属 ⑤酸性氧化物 ⑥酸
A.只有①②③ B.只有①④⑥ C.只有②⑤⑥ D.全部
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | 氢氧化钠的摩尔质量是40g |
|
| B. | 1molNaOH的质量是40g/mol |
|
| C. | 1gH2和1gN2所含分子数相等 |
|
| D. | 阿伏伽德罗常数个钠原子的质量是23g |
查看答案和解析>>
科目:高中化学 来源: 题型:
设计实验证明酸性强弱顺序:HCl>H2CO3>H2SiO3。
(1)写出实验原理的化学反应方程式________________。
(2)设计本实验所依据的化学原理是________________。
(3)实验中必须用到的药品有________________,所需的实验仪器有________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)将碳酸钙、稀盐酸、铁、氧气四种物质填写到下图的适当位置。

(2)从(1)中的四种物质中选出一种或几种为反应物,按下述反应类型,各写一个化学方程式。
①分解反应:__________________________________________。
②化合反应:__________________________________________。
③置换反应:__________________________________________。
④复分解反应:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)实验室中,制取Fe(OH)3胶体的操作方法是_________________________ ,反应方程式是______________________,证明胶体已经制成的方法是
_________________________________________________。
(2)已知Fe(OH)3胶粒带正电荷,Al(OH)3胶粒也带正电荷,而H2SiO3胶粒带负电荷,则下列实验的现象分别是:
①Fe(OH)3胶粒和Al(OH)3胶粒混合:_______________________;
②Fe(OH)3胶粒和H2SiO3胶粒混合:_______________________。
(3)已知Al(OH)3胶体能够净水,则Fe(OH)3胶体____________________(填“能”或“不能”)净水。
查看答案和解析>>
科目:高中化学 来源: 题型:
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为
A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。
B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。
C.氨气分子是极性分子而甲烷是非极性分子。
D.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。
查看答案和解析>>
科目:高中化学 来源: 题型:
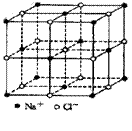
食盐晶体如图所示。在晶体中,· 表示Na+,o 表示Cl-。已知食盐的密度为r g / cm3,NaCl摩尔质量M g / mol,阿伏加德罗常数为N,则在食盐晶体里Na+和Cl-的间距大约是
 |
A. 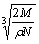 cm B.
cm B. 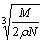 cm
cm
C. 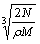 cm D.
cm D. 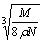 cm
cm
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法中,不正确的是:
A.a mol/L的HCN溶液与b mol/L的NaOH溶液等体积混合,所得溶液中
c(Na+)>c(CN-),则a一定小于b
B.常温下,CH3COONa溶液的pH=8,则c(Na+) -c(CH3COO-)=9.9×10-7mol/L
C.常温下,0.1mol/L的某酸溶液中,若c(OH-)/c(H+) =1×10-8,则溶液中由水电离出的
c(H+) =1×10-11mol/L
D.在0.1 mol/L Na2SO3溶液中加入少量NaOH固体,c(SO32-)与c(Na+)均增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com