
| A、溶液中氢氧根离子的浓度增大了 |
| B、c(CH3COOH)减小,电离平衡向生成醋酸分子的方向移动? |
| C、平衡向电离的方向移动,氢离子的浓度增大,醋酸分子的数量减少 |
| D、电离程度增大,c(CH3COO-)也增大了 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
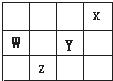
| A、四元素中,X的单质最稳定 |
| B、氢化物稳定性:HY>H2Z |
| C、原子半径:W>Y |
| D、W在周期表中的位置为:第2周期第5族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、吸热反应不加热就不会发生 |
| B、据能量守恒定律,反应物的总能量一定等于生成物的总能量 |
| C、化学反应除了生成新的物质外,还伴随着能量的变化 |
| D、放热的化学反应不需要加热就能发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡时甲、乙两容器体积相等 |
| B、平衡时甲、乙两容器中c(H2)相等 |
| C、平衡时甲、乙两容器中反应速率v(H2)相等 |
| D、平衡时甲、乙两容器中气体总的物质的量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:

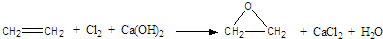

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com