
【题目】下列离子方程式中,能正确表示盐的水解反应的是( )
A.NH4++H2ONH3H2O+H+
B.Fe3++3H2O═Fe(OH)3↓+3H+
C.S2﹣+2H2O═H2S+2OH﹣
D.Br﹣+H2O═HBr+OH﹣
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A. 摩尔是表示物质的量的单位,每摩尔物质含有6.02×1023个分子
B. 2H既可表示2个氢原子,又可表示2 mol氢原子
C. 相同物质的量的CO和CO2所含的原子总数目之比为2∶3
D. 相同质量的CO和CO2所含的原子总数目之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示法不正确的是( )
A.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由C(石墨)→C(金刚石) ΔH = +1.9 kJ·mol—1可知石墨比金刚石稳定
C.在稀溶液中:H++OH- ![]() H2O ΔH =-57.3 kJ·mol—1,若将含1mol CH3COOH的醋酸溶液与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJ
H2O ΔH =-57.3 kJ·mol—1,若将含1mol CH3COOH的醋酸溶液与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJ
D.在热化学方程式中无论是反应物还是生成物必须表明聚集状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据事实,写出下列反应的热化学方程式。
(1)1 mol C2H4(g)与适量O2(g)反应生成CO2(g)和H2O(l),放出1411 kJ能量: 。
(2)1 mol C2H5OH(l)与适量O2(g)反应生成CO2(g)和H2O(l),放出1366.8 kJ热量: 。
(3)2 mol Al(s)与适量O2(g)发生反应生成Al2O3(s),放出1669.8 kJ热量: 。
(4)在200°C、101 kPa时,1 mol H2与碘蒸气作用生成HI气体,放出14.9 kJ热量: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验基本操作中正确的是
A. 稀释浓硫酸时,将浓硫酸沿器壁缓慢注入水中,并不断搅拌
B. 过滤时,漏斗里液体的液面要高于滤纸的边缘
C. 胶头滴管的管口直接伸入试管里滴加液体,以免外溅
D. 实验结束后,用嘴吹灭酒精灯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列递变规律不正确的是( )
A.Na、Mg、Al原子的失电子能力逐渐减弱
B.Si、P、S元素的最高正化合价依次降低
C.C、N、O的原子半径依次减小
D.Cl、Br、I的气态氢化物的稳态性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将氯碱工业与燃料电池联合能够有效降低能源消耗,如图是该工艺的图示(电源及电极未标出),请回答下列问题: 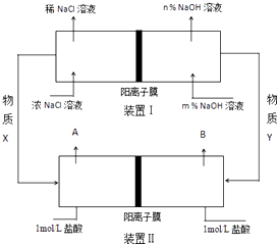
(1)电解饱和食盐水(氯碱工业)的化学方程式为 .
(2)物质X为 , 装置Ⅰ和Ⅱ中属于燃料电池的是 .
(3)装置Ⅰ中,NaOH溶液浓度m%n% (填“>”或“<”).
(4)利用装置Ⅱ可获得10mol/L盐酸,该产品出口为(填“A”或“B”),请说明理由 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如表所示:
化学式 | HF | H2CO3 | HClO |
电离平衡常数(Ka) | 7.2×10﹣4 | K1=4.4×10﹣7 | 3.0×10﹣8 |
(1)将浓度为0.1molL﹣1 HF溶液加水稀释一倍(假设温度不变),下列各量增大的是 .
A.c(H+)
B.c(H+)c(OH﹣)
C.![]()
D.![]()
(2)25℃时,在20mL 0.1molL﹣1氢氟酸中加入V mL 0.1molL﹣1 NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是 . 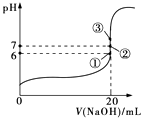
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中c(F﹣)﹣c(Na+)=9.9×10﹣7 molL﹣1
C.②点时,溶液中的c(F﹣)=c(Na+)
D.③点时V=20mL,此时溶液中c(F﹣)<c(Na+)=0.1molL﹣1
(3)物质的量浓度均为0.1molL﹣1的下列四种溶液:①Na2CO3溶液;②NaHCO3溶液;③NaF溶液;④NaClO溶液.依据数据判断pH由大到小的顺序是 .
(4)Na2CO3溶液显碱性是因为CO32﹣水解的缘故,请设计简单的实验事实证明之 .
(5)长期以来,一直认为氟的含氧酸不存在.1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H﹣O﹣F.HFO与水反应得到HF和化合物A,每生成1mol HF转移mol电子.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com