
(14分)(1)下图是工业氮气和氢气合成1mol氨气过程中能量变化示意图,

请写出该反应的热化学方程式 。
(2)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=C02(g) △H1=-393.5kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H3=-2599kJ·mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变:△H=____ 。
(3)将铁片和锌片放在盛有NaCl溶液(其中滴有酚酞)的表面皿中,如下图所示。

正极上发生的电极反应为___
阴极上发生的电极反应为___
(4)如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是________(填“a”或“b”)极,负极的电极反应式是 __ _。
②电池工作一段时间后电解质溶液的pH______(填“增大”、“减小”或“不变”)
(1)N2(g)+3H2 (g)===2NH3(g) ΔH=2(a-b)kJ/mol
(2)226.7kJ·mol-1 (3) 2H2O+O2 +4e-==4OH- 2H++2e-==H2↑
(4)①a CH4+10OH-―8e-=CO32-+7H2O ②减小
【解析】
试题分析:(1)①由图1可知,1molN2(g)与3molH2(g)完全反应生成2molNH3(g)的反应热为508kJ/mol-600kJ/mol=-92kJ/mol,所以合成氨的热化学反应方程式为:N2(g)+3H2 (g)2NH3(g)△H=-92kJ/mol,故答案为:N2(g)+3H2(g)
(g)2NH3(g)△H=-92kJ/mol,故答案为:N2(g)+3H2(g) 2NH3(g)△H=-92kJ/mol。
2NH3(g)△H=-92kJ/mol。
(2)已知:①C (s,石墨)+O2(g)=CO2(g)△H1=-393.5kJ?mol-1;
②2H2(g)+O2(g)=2H2O (l)△H2=-571.6kJ?mol-1;
③2C2H2(g)+5O2(g)═4CO2(g)+2H2O (l)△H2=-2599kJ?mol-1;
2C (s,石墨)+H2(g)=C2H2(g)的反应可以根据①×2+②×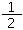 -③×
-③×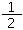 得到,所以反应焓变△H=2×(-393.5kJ?mol-1)+(-571.6kJ?mol-1)×
得到,所以反应焓变△H=2×(-393.5kJ?mol-1)+(-571.6kJ?mol-1)×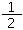 -(-2599kJ?mol-1)×
-(-2599kJ?mol-1)×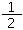 =+226.7kJ?mol-1,故答案为:△H=+226.7kJ?mol-1.
=+226.7kJ?mol-1,故答案为:△H=+226.7kJ?mol-1.
(3) 甲图示是原电池,锌做负极,锌失电子形成锌离子,正极是Ⅰ,在正极上,O2+2H2O+4e-=4OH-;所以Ⅰ处变红;乙图示是电解池,铁做阳极,铁失电子生成亚铁离子,锌做阴极,在阴极上,2H++2e-=H2↑,破坏了锌片附近水的电离平衡,使得OH-浓度增大,所以Ⅳ处也变红.故答案为:2H2O+O2 +4e-==4OH- 2H++2e-==H2↑
(4)由原电池原理确定a极为负极,电极反应式为CH4+10OH--8e-==CO32-+7H2O;正极反应式为2O2+4H2O+8e-==8OH-;合并的原电池的总反应式为CH4+2OH-+2O2==3H2O+ CO32-;确定工作一段时间后溶液的p H会减小;故答案为:①a CH4+10OH-―8e-=CO32-+7H2O ②减小
考点:热化学方程式的书写、盖斯定律的应用、原电池和电解池的工作原理、简单实验及p H的计算。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015浙江省高一1月月考化学试卷(解析版) 题型:选择题
将标准状况下a L HCl(g)溶于100g水中,得到的盐酸的密度为b g·cm-3,则该盐酸的物质的量浓度是
A. mol·L-1
mol·L-1
B. mol·L-1
mol·L-1
C. mol·L-1
mol·L-1
D. mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高二1月月考化学试卷(解析版) 题型:选择题
下列关于催化剂说法正确的是
A.任何化学反应都需要催化剂
B.催化剂能使不反应的物质之间发生反应
C.催化剂在化学反应前后,化学性质和质量都不变
D.电解水时加少量的NaOH做催化剂,可使电解速率加快
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省淄博市高二12月月考化学试卷(解析版) 题型:选择题
醋酸溶液中存在电离平衡:CH3COOH H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是
A、醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-)
B、0.10mol/L的CH3COOH溶液加水稀释,溶液中c(OH-)减小
C、CH3COOH溶液中加入少量的CH3COONa固体,平衡逆向移动
D、常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省淄博市高二12月月考化学试卷(解析版) 题型:选择题
下列措施能加快Fe与0.1mol/L的稀H2SO4反应产生H2的反应速率的是
A.向溶液中再滴加1mol/L的HNO3 B.将稀硫酸改为98%的浓硫酸
C.滴加少量的CuSO4 溶液 D.降低温度
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省平度市高二上学期期中考试化学试卷(解析版) 题型:选择题
在密闭容器中一定量混合气体发生反应:2A (g) + B (g)) xC(g),达到平衡时测得 A的浓度为 0.5 mol/L,在温度不变的条件下,将容器的容积扩大到原来的2倍, 再达平衡时测得A的浓度为 0.3 mol/L ,下列有关判断正确的是
xC(g),达到平衡时测得 A的浓度为 0.5 mol/L,在温度不变的条件下,将容器的容积扩大到原来的2倍, 再达平衡时测得A的浓度为 0.3 mol/L ,下列有关判断正确的是
A.x = 3 B.平衡向正反应方向移动
C.B的转化率降低 D.C的体积分数增大
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省平度市高二上学期期中考试化学试卷(解析版) 题型:选择题
下列依据热化学方程式得出的结论正确的是
A.已知2H2(g)+O2(g)=2H2O(l),△H=-483.6 kJ·mol–1,则 2molH2(g)和1molO2(g)所含有的总能量比2mol H2O(l)所含有的总能量少483.6kJ
B.己知2C(s)+2O2(g)=2CO2(g)△H1 2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2
C.已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定
D.利用盖斯定律可以间接计算通过实验难以测定反应的反应热
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高二上学期期中考试化学试卷(解析版) 题型:选择题
下列与盐类水解有关,不正确的是
A.对于0.1 mol·L-1Na2SO3溶液,升高温度,溶液pH增大
B.在NH4Cl或AlCl3溶液中加入镁条会产生气泡;
C.均不能采取将溶液直接蒸干的方法制得MgCl2、Al2(SO4)3、FeCl3、Fe2(SO4)3
D.为保存FeCl3溶液,要在溶液中加入少量盐酸;
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高一12月月考化学试卷(解析版) 题型:选择题
在某无色酸性溶液中能大量共存的一组离子是
A.NH4+、SO42- 、Al3+、NO3- B.Na+、K+、HCO3-、NO3-
C.Na+ 、Ca2+ 、NO3- 、CO32- D.K+、Cu2+、NH4+、NO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com