
| 2.3g |
| 23g/mol |
| n |
| V |
| 2.3g |
| 23g/mol |
| 1 |
| 2 |
| 0.1mol |
| 0.2L |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
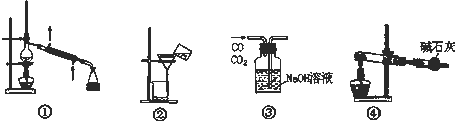
| A、装置①常用于分离沸点不同,且彼此互溶的液态混合物 |
| B、装置②常用于过滤操作 |
| C、装置③可用于除去CO中混有的CO2气体 |
| D、装置④可用于以NaHCO3为原料实验室制备CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑤ | B、①③⑥ |
| C、②④⑤ | D、①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 牙膏品牌 | X牙膏 | Y牙膏 | Z牙膏 |
| 摩擦剂 | 氢氧化钠 | 碳酸钙 | 二氧化硅 |
| 摩擦剂的物质类别(指酸、碱、盐、氧化物) |

查看答案和解析>>
科目:高中化学 来源: 题型:
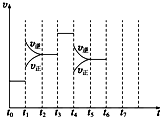 在一密闭容器中发生反应N2+3H2?2NH3△H<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
在一密闭容器中发生反应N2+3H2?2NH3△H<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
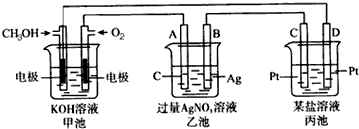
查看答案和解析>>
科目:高中化学 来源: 题型:
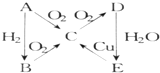 如图所示A、B、C、D、E五种种物质的相互转化关系:
如图所示A、B、C、D、E五种种物质的相互转化关系:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com