
| A. | 四氯化碳-非电解质 氯化银-强电解质 碳酸-弱电解质 | |
| B. | NO2-酸性氧化物 CuO-碱性氧化物 Al2O3-两性氧化物 | |
| C. | 冰醋酸、纯碱、芒硝、生石灰分别属于酸、碱、盐、氧化物 | |
| D. | 碘酒、淀粉溶液、水雾、纳米材料均为胶体 |
分析 A.在水溶液里或熔融状态下完全电离的是强电解质,部分电离的是弱电解质;在水溶液里或熔融状态下不导电的化合物是非电解质,单质和混合物既不是电解质,也不是非电解质;
B.能和碱反应生成盐和水的氧化物属于酸性氧化物;能跟酸起反应,生成盐和水的氧化物是碱性氧化物;既可以与酸反应生成盐和水又可以与碱反应生成盐和水的氧化物称为两性氧化物;
C.纯碱是碳酸钠属于盐;
D.胶体的本质特征是分散质微粒直径在1nm-100nm间.
解答 解:A.四氯化碳是在水溶液里或熔融状态下不导电的化合物,是非电解质;氯化银在熔融状态下完全电离,属于强电解质;碳酸在水溶液里只能部分属于弱电解质,故A正确;
B.NO2不是酸性氧化物,CuO是碱性氧化物 Al2O3是两性氧化物,故B错误;
C.纯碱是碳酸钠属于盐,不是碱,故C错误;
D.碘酒是碘单质的酒精溶液,不是胶体,故D错误;
故选A.
点评 本题考查了物质分类,电解质、酸、碱、盐、氧化物等概念分析,胶体性质分析应用,掌握基础是关键,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 节日期间,在任意场所燃放烟花爆竹 | |
| B. | 实验时,将水倒入浓硫酸配置稀硫酸 | |
| C. | 煤矿矿井,必须通风,严禁烟火 | |
| D. | 用点燃的火柴在液化气钢瓶口检验是否漏气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.8L0.1mol•L-1的KCl溶液 | B. | 0.2L0.2mol•L-1的HCl溶液 | ||
| C. | 0.3L0.2mol•L-1的MgCl2溶液 | D. | 0.5L 0.1mol•L-1的AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | Na2O2与 H2O反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| C. | 氯气与水反应:Cl2+H2O═Cl-+2H++ClO- | |
| D. | 碳酸镁与稀盐酸反应:MgCO3+2H+═Mg2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,单位物质的量的气体所占的体积就叫气体的摩尔体积 | |
| B. | 物质的量是表示一定数目粒子集合体的一个物理量 | |
| C. | 0.012kg的碳中所含的碳原子数就是阿伏伽德罗常数 | |
| D. | Al原子的摩尔质量为27g,Al3+因少了3个电子,摩尔质量更小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢原子的结构示意图为: ;则反氢原子的结构示意图为: ;则反氢原子的结构示意图为: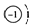 | |
| B. | 反氢原子中有一个带负电荷的反质子和一个带正电荷的反电子 | |
| C. | 反氢原子的摩尔质量为1g/mol | |
| D. | 21H的反氢原子中有2个带负电荷的反质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
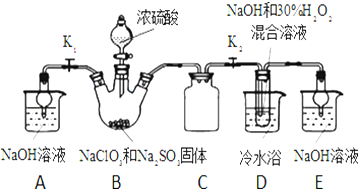
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com