
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,1个氧气分子体积为 ![]() cm3
cm3
B.铜电解精炼时,当阳极质量减少64 g时,电路中转移电子数为2NA
C.标准状况下22.4 L Cl2完全溶于水时,所得溶液中含氯微粒总数为2NA
D.NaCl晶体中Na+与最近Cl-的核间距离为a cm,则其晶体密度为 ![]() g·cm-3
g·cm-3
【答案】D
【解析】
A. 标准状况下,1个氧气分子体积由氧气分子的大小决定不能直接用气体摩尔体积进行计算,故A错误;
B. 铜电解精炼时,阳极中含有Cu、Fe、Zn等金属,Fe、Zn先放电,当阳极质量减少64 g时,电路中转移电子数不等于2NA,故B错误;
C. 标准状况下22.4 L Cl2物质的量为1mol完全溶于水时,所得溶液中含氯微粒有Cl2、HClO、Cl-、ClO-,根据氯原子守恒可知:![]() , 则含氯微粒总数小于2NA,故C错误;
, 则含氯微粒总数小于2NA,故C错误;
D. NaCl晶胞中Na+数目为![]() , Cl-数目为
, Cl-数目为![]() ,则晶胞质量为:
,则晶胞质量为:![]() ,与最近Cl-的核间距离为a cm,则体积为
,与最近Cl-的核间距离为a cm,则体积为![]() ,则其晶体密度为
,则其晶体密度为 ![]() g·cm-3,故D正确;
g·cm-3,故D正确;
故答案选:D。


 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
【题目】如图表示细胞内某些有机物的元素组成和功能关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子,X、Y、Z、P分别为构成生物大分子的基本单位,请回答下列问题:

(1)Ⅰ在小麦种子中主要是指________,其单体X为_________是细胞生命活动所需的主要能源物质。
(2)物质Ⅲ是_______,其元素组成有___________等。
(3)在细胞中含量最高的有机物是___________(填字母),它能与双缩脲试发生作用,产生_____色反应。(4)物质Y是___________,组成Ⅱ的Y有4种,Y的种类与组成它的_________种类有关。
(5)细胞内良好的储能物质是_______,它属于脂质,脂质还有两类物质,其中________是细胞膜及细胞器膜等的重要成分,而固醇包括胆固醇、________和______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.2 L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题
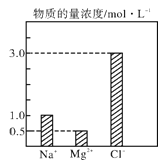
(1)该混合液中,NaCl的物质的量为_________mol,含溶质MgCl2的质量为_______g。
(2)该混合液中CaCl2的物质的量为___________mol,将该混合液加水稀释至体积为1 L,稀释后溶液中Ca2+的物质的量浓度为__________mol·L-1。
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸氯喹是一种抗疟疾药物,研究表明该药物对新型冠状病毒2019-nCOV有较好抑制作用,以下是该药物主体氯喹的合成路线。
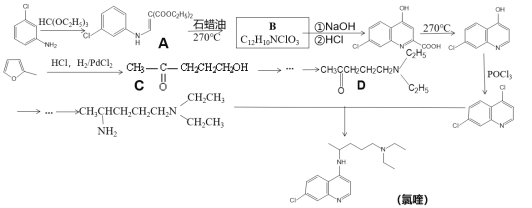
已知:①![]() 具有芳香性;
具有芳香性;
②R1-Cl+H2N-R2 → R1-NH-R2+HCl
请回答:
(1)下列说法不正确的是_________
A.氯喹具有弱碱性 B.氯喹的分子式为C18H24N3Cl
C.整个合成过程中包含了取代、加成反应 D.1molB最多可以消耗3molNaOH
(2)请写出A转化成B的化学方程式_________
(3)A转化成B的过程中还会生成一种双六元环副产物,其结构简式为_________
(4)请利用乙烯为原料将合成路线中C→D部分补充完整,用线路图表示出来(无机试剂任选)_________
(5)请写出满足下列条件的![]() 的同分异构体_________
的同分异构体_________
①1HNMR谱显示分子中只存在两种H;②分子内只存在一个环结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】缺电子化合物是指电子数不符合路易斯结构(一个原子通过共享电子使其价层电子数达到8,H原子达到2所形成的稳定分子结构)要求的一类化合物。下列说法错误的是
A.NH3、BF3、BF4-中只有BF3是缺电子化合物
B.BF3、BF4-中心原子的杂化方式分别为sp2、sp3
C.BF3与NH3反应时有配位键生成
D.BF4-的键角小于NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Al2H6燃烧热极高,是一种很好的生氢剂,它跟水反应生成H2,球棍模型如图(白球为Al,黑球为H).下列推测肯定不正确的是( )

A. 该物质与水反应,属于氧化还原反应
B. Al2H6在空气中完全燃烧,产物为氧化铝和水
C. Al2H6分子中 氢为+1价,铝为﹣3价
D. 氢铝化合物可能成为未来的储氢材料和火箭燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子或离子中,价层电子对互斥模型(简称VSEPR模型),VSEPR模型几何构型与分子或离子的立体构型不一致的是( )
A. CO2B. H2OC. CO32﹣D. CCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I是合成含六元环甾类化合物的一种中间体。利用Robinson成环反应合成I的路线如下,回答下列问题:

已知:①![]()
②
(1)B→C的反应方程式为________。
(2)化合物E和I的结构简式分别是________、________。
(3)C→D和F→G的反应类型分别是________、________。
(4)写出符合下列条件的G的同分异构体的结构简式________。
①与氢氧化钠完全反应时,二者物质的量之比为1:3;②有4种不同化学环境的氢。
(5)写出以甲醇、苯甲酸、乙酸甲酯和![]() 为原料合成
为原料合成 的合成路线(其它试剂任选)。______________________________________。
的合成路线(其它试剂任选)。______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组以废弃的易拉罐、漂白粉、氢氧化钠等为原料制造了一种新型环保电池,并进行相关实验,如图所示。电池的总反应方程式为2Al+3ClO-+2OH-=3Cl-+2AlO![]() +H2O。下列说法正确的是
+H2O。下列说法正确的是
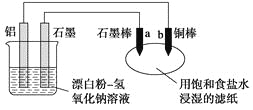
A. 电池的负极反应式为:ClO-+H2O+2e-=Cl-+2OH-
B. 当有0.1 mol Al完全溶解时,流经电解液的电子数为1.806×1023个
C. 往滤纸上滴加酚酞试液,b极附近颜色变红
D. b极附近会生成蓝色固体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com