
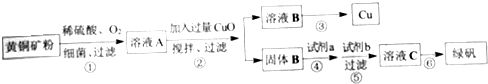
分析 根据生产铜和绿矾的工艺可知,黄铜矿先氧化成硫酸盐,得溶液A,再加故氧化铜调节溶液的PH值,得固体B为氢氧化铁沉淀和溶液B,溶液B中含有铜离子,再通过还原反应得铜单质,氢氧化铁再用稀硫酸溶解,再用铁粉还可得C为硫酸亚铁溶液,再通过蒸发浓缩、降温结晶得绿矾,
(1)根据化合价代数为0可判断黄铜矿CuFeS2中Cu的化合价;
(2)根据元素守恒和电荷守恒写化学方程式,根据炼铜时的耗能和环保的角度分析;
(3)加入过量氧化铜调节溶液PH,使铁离子变成氢氧化铁沉淀;
(4)加入稀硫酸溶解氢氧化铁生成硫酸铁,加入铁粉和硫酸铁反应生成硫酸亚铁;
(5)从溶液中获得绿矾晶体需要经过蒸发浓缩、冷却结晶、过滤操作、洗涤干燥;
(6)湿法炼铜就是用铁转换出铜.
解答 解:根据生产铜和绿矾的工艺可知,黄铜矿先氧化成硫酸盐,得溶液A,再加故氧化铜调节溶液的PH值,得固体B为氢氧化铁沉淀和溶液B,溶液B中含有铜离子,再通过还原反应得铜单质,氢氧化铁再用稀硫酸溶解,再用铁粉还可得C为硫酸亚铁溶液,再通过蒸发浓缩、降温结晶得绿矾,
(1)根据化合价代数为0可知黄铜矿CuFeS2中Cu的化合价为+2,
故答案为:+2;
(2)反应①的化学方程式为 4CuFeS2+17O2+2H2SO4=4CuSO4+2Fe2(SO4)3+2H2O,生物湿法炼铜与高温炼铜相比,它的优点有不需要加热,耗能少,没有二氧化硫等尾气产生等,
故答案为:4CuFeS2+17O2+2H2SO4=4CuSO4+2Fe2(SO4)3+2H2O;不需要加热,耗能少,没有二氧化硫等尾气产生;
(3)加入过量氧化铜调节溶液PH,使铁离子变成氢氧化铁沉淀,
故答案为:调节混合溶液的pH,使Fe3+完全沉淀;
(4)制取的是绿矾,溶解氢氧化铁应该选用稀硫酸,还原铁离子,不能引进新的杂质,最佳选择是铁粉,
故答案为:稀硫酸;铁粉;
(5)获得的滤液经过蒸发浓缩、冷却结晶、过滤、洗涤干燥,最后得到绿矾,
故答案为:蒸发浓缩、冷却结晶;
(6)我国早在西汉时期,就有湿法炼铜的记述:“曾青得铁则化为铜”,该湿法炼铜就是用铁转换出铜,与题中流程中的步骤③一致,
故答案为:③.
点评 本题考查了工业生成铜和绿矾的工业流程,涉及了实验操作、化学方程式书写、溶液PH的调节等知识,本题难度中等.


 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 将废弃塑料直接填埋 | B. | 对废弃塑料回收再利用 | ||
| C. | 用布袋代替塑料袋 | D. | 使用新型可降解塑料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
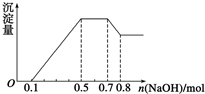 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )| A. | 溶液中的阳离子只有H+、Mg2+、Al3+ | |
| B. | 溶液中n(NH4+)=0.1mol | |
| C. | 溶液中一定不含CO32-,可能含有SO42-和NO3- | |
| D. | n(H+):n(Al3+):n(Mg2+)=2:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中滴加KSCN溶液,若溶液出现血红色则说明原溶液中含Fe3+ | |
| B. | 向某溶液中滴加BaCl2溶液,若有白色沉淀,再滴加足量稀HNO3,若沉淀不溶解,则说明原溶液中一定含Ag+ | |
| C. | 向某溶液中滴加足量稀HCl,产生气体能使澄清石灰水变浑浊,则说明原溶液中一定含CO32- | |
| D. | 向某溶液中滴加NaOH溶液,除溶液体积增大外,无其它现象,说明该溶液与NaOH溶液不反应. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和汽油都是可再生能源,应大力推广使用乙醇汽油 | |
| B. | 二氧化氯具有还原性,可用于自来水的杀菌消毒 | |
| C. | 神舟飞船所用太阳能电池板可将光能转换为电能,所用转换材料是单晶硅 | |
| D. | “辽宁舰”上用于舰载机降落拦阻索的是一种特种钢缆,属于新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x的原子半径大于y的原子半径 | |
| B. | x的电负性大于y的电负性 | |
| C. | x的核电荷数大于y的核电荷数 | |
| D. | x的第一电离能小于y 的第一电离能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH3与Cl2在光照下发生取代反应 | |
| B. | CH3CH=CHCH3与Br2在四氯化碳溶液里发生加成反应 | |
| C. | CH3-CH=CH2和HCl发生加成反应 | |
| D. | 甲苯与溴混合后再加入铁粉时发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com