
| A. | 将SO2气体通入含有氢氧化钠的酚酞溶液中,溶液褪色 | |
| B. | 将SO2气体通入澄清石灰水中,溶液变浑浊 | |
| C. | 将SO2通入品红溶液中,溶液褪色 | |
| D. | 将SO2气体通入碘水溶液中,溶液褪色 |
分析 能体现二氧化硫具有还原性,说明二氧化硫在反应中失电子化合价升高,作还原剂,还原剂体现还原性,据此分析解答.
解答 解:A.发生的反应为SO2+2NaOH=Na2SO3+H2O,该反应中各元素化合价不变,不属于氧化还原反应,故A错误;
B.SO2+Ca(OH)2=CaSO3↓+H2O,该反应中各元素化合价不变,不属于氧化还原反应,故B错误;
C.二氧化硫和有色物质反应生成无色物质而体现漂白性,故C错误;
D.SO2+I2+2H2O=H2SO4+2HI中S元素化合价由+4价变为+6价、I元素化合价由0价变为-1价,所以二氧化硫是还原剂、碘是氧化剂,则二氧化硫体现还原性,故D正确;
故选D.
点评 本题以二氧化硫为载体考查氧化还原反应,侧重考查基本理论,明确元素化合价变化是解本题关键,知道常见元素化合价,注意D中发生的反应,为易错点.


 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:填空题
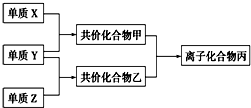 常温下由三种短周期元素形成的气体单质X、Y、Z,并有下列转化关系(反应条件已略去):已知:X分子中含共价键最多;甲分子中含10个电子,乙分子含有18个电子.
常温下由三种短周期元素形成的气体单质X、Y、Z,并有下列转化关系(反应条件已略去):已知:X分子中含共价键最多;甲分子中含10个电子,乙分子含有18个电子. ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | 391 | 945 |
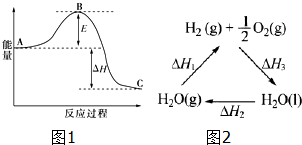
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn | B. | 碳棒 | C. | MnO2 | D. | MnO2和H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
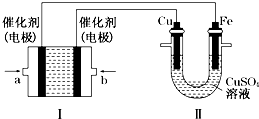 甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:
甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
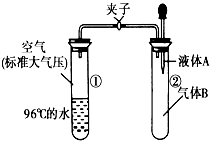 如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了,则液体A和气体B的组合不可能是下列的( )
如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了,则液体A和气体B的组合不可能是下列的( )| A. | 氢氧化钠溶液、二氧化碳 | B. | 水、氨气 | ||
| C. | 氢氧化钠溶液、一氧化氮 | D. | 水、二氧化氮 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液(Na2CO3),应通入过量的CO2气体 | |
| B. | NaBr溶液(NaI),应加入适量的氯水、CCl4,进行萃取分液 | |
| C. | NH4Cl溶液(FeCl3),应加入适量的氨水,过滤 | |
| D. | CO2(CO),通过过量的灼热的氧化铜粉末 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 现象或事实 | 解释 |
| A | 蔗糖、淀粉、纤维素等有甜味 | 人体内,糖类在淀粉酶的作用下能发生水解,生成葡萄糖 |
| B | 煤通过气化和液化等化学变化可以有效地控制酸雨 | 煤通过气化和液化处理,其产品中硫的含量将大大降低 |
| C | 地沟油经过处理加工后可用作飞机、汽车燃油 | 地沟油的成分是液态烃 |
| D | 在钢铁制品的表面镀上一层锡,可有效防止其被腐蚀 | 形成原电池时锡是负极被氧化,而钢铁制品作为正极被保护 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com