
氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:
(1)氨的水溶液显弱碱性,其原因为 (用离子方程式表示),0.1 mol·L-1的氨水中加入少量的NH4Cl固体,溶液的PH (填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度 (填“增大”或“减小”)。
 (2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为 ,平衡常数表达式为 ;若有1mol硝酸铵完全分解,转移的电子数为 mol。
(2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为 ,平衡常数表达式为 ;若有1mol硝酸铵完全分解,转移的电子数为 mol。
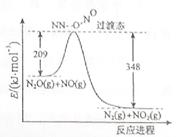
(3)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1molN2, 其△H= kJ·mol-1。
【答案】(1)NH3·H2O NH4++OH- 降低 增大;;
NH4++OH- 降低 增大;;
(2)NH4NO3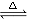 N2O+2H2O;c(N2O)c(H2O)2;4
N2O+2H2O;c(N2O)c(H2O)2;4
 (3)-139
(3)-139
【解析】(1)氨水中的一水合氨部分电离产生铵根离子和氢氧根离子,使溶液显碱性;若加入氯化铵,则铵根离子浓度增大,一水合氨的电离平衡逆向移动,氢氧根离子浓度减小, pH降低;若加入少量的明矾,铝离子水解呈酸性,抑制铵离子水解,溶液中的NH4+的浓度增大;
(2)根据题意可书写反应的化学方程式,注意为可逆反应;根据平衡常数的定义可书写该反应的平衡常数表达式,硝酸铵为固体,不能表示平衡常数;硝酸铵中N元素的化合价从+5价降低到-1价或从-3价升高到+1价,均转移4个电子,所以生成1mol氮气则转移4mol电子;
(3)根据图像可知N2O与NO反应生成氮气和二氧化氮的反应热为(209-348)kJ/mol=-109kJ/mol。
【考点定位】本题考查弱电解质的电离平衡的判断,化学方程式的书写,化学反应与能量的关系判断。
【名师点睛】以氨气、硝酸铵和氮的氧化物为载体考查弱电解质电离平衡的影响因素、化学方程式的书写、平衡常数表达式的书写、氧化还原反应电子转移的数目及反应热的计算。以元素化合物知识为载体考查基本概念和基本原理是高考命题的主旨,考查考查学生分析问题、解决问题的能力,是化学高考的常见题型。题目难度中等。


科目:高中化学 来源: 题型:
一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g) 
 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
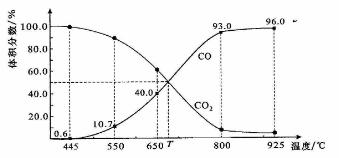
已知:气体分压(P分)=气体总压(P总)×体积分数。下列说法正确的是( )
A.550℃时,若充入惰性气体,ʋ正,ʋ逆 均减小,平衡不移动
B.650℃时,反应达平衡后CO2的转化率为25.0%
C.T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动
D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数KP=24.0P总
查看答案和解析>>
科目:高中化学 来源: 题型:
50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。试回答下列问题:
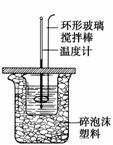
(1)大小烧杯间填满碎纸条的作用是
________________________________________________________________________。
(2)大烧杯上如不盖硬纸板,求得的中和热数值将________(填“偏大”、“偏小”或“无影响”)。结合日常生活的实际该实验在______中进行效果更好。
(3)实验中改用60 m L 0.50 mol·L-1盐酸与 50 m L 0.55 mol·L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),所求中和热________(填“相等”或“不相等”),简述理由__________________________________________。
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会________;用50 m L 0.5 mol·L-1 NaOH溶液进行上述实验,测得的中和热的数值会
________________________________________________________________________。
(均填“偏大”、“偏小”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
今有如下三个热化学方程式:
H2(g)+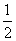 O2(g)===H2O(g) ΔH=a kJ·mol-1
O2(g)===H2O(g) ΔH=a kJ·mol-1
H2(g)+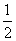 O2(g)===H2O(l) ΔH=b kJ·mol-1
O2(g)===H2O(l) ΔH=b kJ·mol-1
2H2(g)+O2(g)===2H2O(l) ΔH=c kJ·mol-1
下列关于他们的表述正确的是( )
A.它们都是吸热反应 B.a、b和c均为正值
C.a=b D.2b=c
查看答案和解析>>
科目:高中化学 来源: 题型:
最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:
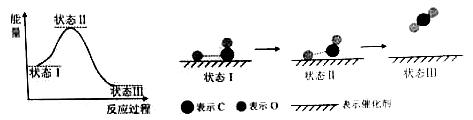
下列说法中正确的是( )
A.CO和O生成CO2是吸热反应
B.在该过程中,CO断键形成C和O
C.CO和O生成了具有极性共价键的CO2
D.状态Ⅰ →状态Ⅲ表示CO与O2反应的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学用语表示正确的是( )
A.乙烯的结构简式:CH2CH2
B.乙烯的分子式:C2H4
C.乙酸的结构简式:C2H4O2
D.甲醛的电子式: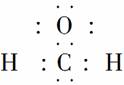
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.分子式为CH4O和C2H6O的物质一定互为同系物
B.甲烷、乙烯和苯在工业上都可通过石油分馏得到
C.苯酚钠溶液中通入少量二氧化碳生成苯酚和碳酸钠
D.1 mol 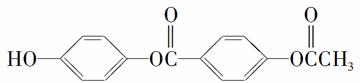 与过量的NaOH溶液加热充分反应,能消耗5 mol NaOH
与过量的NaOH溶液加热充分反应,能消耗5 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
维生素C的结构简式为
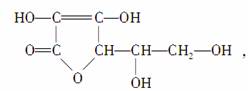 丁香油酚的结构简式为:
丁香油酚的结构简式为:
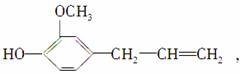 下列关于两者的说法正确的是( )
下列关于两者的说法正确的是( )
A.均含酯基 B.均含醇羟基和酚羟基
C.均含碳碳双键 D.均为芳香化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )。
A.1molH2O中含有的原子数为NA
B.2gH2中含有的氢原子数为2NA
C.常温常压下,11.2LN2中含有的分子数为0.5NA
D.1L0.1mol·L-1 NaNO3溶液中含有的钠离子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com