
 氧化剂或氯化剂,能与许多有机物反应。请回答下列问题:
氧化剂或氯化剂,能与许多有机物反应。请回答下列问题: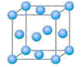
 分子的空间构型是_______。
分子的空间构型是_______。 成的合金。
成的合金。 态碳(C)原子的价电子排布式为 。
态碳(C)原子的价电子排布式为 。 )4分解为Ni和CO,从而制得高纯度的Ni粉。试推测:四羰基镍的晶体类型是 , Ni(CO)4易溶于 (填序号)。
)4分解为Ni和CO,从而制得高纯度的Ni粉。试推测:四羰基镍的晶体类型是 , Ni(CO)4易溶于 (填序号)。 种元素的晶体竟然具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方密堆积,试写出该晶体的化学式 。晶体中
种元素的晶体竟然具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方密堆积,试写出该晶体的化学式 。晶体中 每个镁原子周围距离最近的镍原子有 个。
每个镁原子周围距离最近的镍原子有 个。
科目:高中化学 来源:不详 题型:单选题
| A.附着在试管内壁上的AgCl固体可用氨水溶解而洗去 |
| B.可用氨水鉴别AlCl3、AgNO3和CuSO4三种溶液 |
| C.向氨水中滴加CuSO4溶液至过量,先产生蓝色沉淀,然后沉淀溶解并得到深蓝色溶液 |
| D.加热碘单质,产生紫色碘蒸气,这个过程只克服范德华作用力 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子化合物熔沸点较高、共价化合物熔沸点较低 |
| B.非金属原子间不可能形成离子化合物 |
| C.确定某化合物为离子化合物,可以用融化时能否导电来判断 |
| D.共价化合物中可能有离子键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素代号 | W | R | X | Y | Z | Q | M |
| 原子半径/nm | 0.037 | 0.186 | 0.074 | 0.075 | 0.077 | 0.110 | 0.160 |
| 主要化合价 | +1 | +1 | -2 | -3,+5 | +2,+4 | -3,+5 | +2 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SiCl4、PCl5分子中各原子最外层均达到8电子稳定结构 |
| B.化学反应中能量变化的大小与反应物的质量多少无关。 |
| C.经实验测得邻-二溴苯仅一种结构,说明苯环结构中,不存在单双键交替结构 |
| D.需要加热才能发生的反应一定是吸热反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 O)4和 [Cu(NH3)4]2+,[Fe(SCN)]2+配合物离子中,提供空轨道接受孤对电子的原子或离子分别是:_______________、___________、___ __________。
O)4和 [Cu(NH3)4]2+,[Fe(SCN)]2+配合物离子中,提供空轨道接受孤对电子的原子或离子分别是:_______________、___________、___ __________。 ,BCl3的空间构型为:___________
,BCl3的空间构型为:___________ 子
子 的化学式:(只需写一种)
的化学式:(只需写一种)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 物质 | Na2O | NaCl | AlF3 | AlCl3 | BCl3 | Al2O3 | CO2 | SiO2 |
| 熔点 | 920 | 801 | 1291 | 190 | —107 | 2073 | —57 | 1723 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.同周期元素中X的金属性最强 | B.同族元素中Z的氢化物沸点最高 |
| C.原子半径X>Y,离子半径X+> Z2— | D.Y的单质和氧化物有相同的晶体类型 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2SO4 | B.H2CO3 | C.HNO3 | D.H2SiO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com