
| A. | ①②③ | B. | ①③⑤ | C. | ②④⑤ | D. | ③⑤ |
分析 第七周期排满,最后一种元素的元素序数为118,为零族元素,则116号元素位于ⅥA族,为氧族元素,原子最外层电子数为6,最高正价为+6价,同主族自上而下金属性增强、非金属性减弱,最高价氧化物对应的水化物的酸性减弱.
解答 解:如第七周期排满,最后一种元素的元素序数为118,为零族元素,则116号元素R位于ⅥA族,为氧族元素.
①同主族自上而下金属性增强、非金属性减弱,116号元素为金属元素,不能与Na形成化合物,故①错误;
②同主族元素从上到下元素的非金属性逐渐减弱,金属性逐渐增强,其最高价氧化物的水化物应呈碱性,故②错误;
③同主族元素从上到下元素的金属性逐渐增强,第六周期元素为Po,属于金属元素,则116号元素肯定为金属元素,故③正确;
④由③分析可知R为金属元素,故④错误;
⑤R位于ⅥA族,为氧族元素,原子最外层电子数为6,故⑤正确,
故选D.
点评 本题考查元素周期表和元素周期律知识,题目难度不大,注意正确判断元素在周期表中的位置是解答该题的关键,学习中注意把握元素周期律的递变规律.


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 一定有乙烷 | B. | 一定有丙烷 | ||
| C. | 可能是乙烷和丙烷的混合物 | D. | 可能是甲烷和丁烷的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | C | |
| B |
| A. | A、B、C三元素的气态氢化物溶于水均显酸性 | |
| B. | A、B两种元素的气态氢化物均能与它们的最高价氧化物对应的水化物发生反应,且反应类型相同 | |
| C. | C在周期表中的位置为第二周期第ⅦA族,最高价为+7价 | |
| D. | B02是酸性氧化物,AO2不是酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的氯气与乙烷在光照条件下反应(氯乙烷) | |
| B. | 乙烯与氯气反应(1,2-二氯乙烷) | |
| C. | 液溴与苯用溴化铁作催化剂反应(溴苯) | |
| D. | 乙烯与水反应(乙醇) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 单质 | A | B | C | D | E | F | G | H | I | J |
| 熔点(℃ | -150 | 550 | 160 | 210 | -50 | 370 | 450 | 300 | 260 | 250 |
| 与水反应 | ∨ | ∨ | ∨ | ∨ | ||||||
| 与酸反应 | ∨ | ∨ | ∨ | ∨ | ∨ | ∨ | ||||
| 与氧气反应 | ∨ | ∨ | ∨ | ∨ | ∨ | ∨ | ∨ | ∨ | ||
| 不发生化学反应 | ∨ | ∨ | ||||||||
| 相对于A元素的原子质量 | 1.0 | 8.0 | 15.6 | 17.1 | 23.8 | 31.8 | 20.0 | 29.6 | 3.9 | 18.0 |
| A | ||||||||||
| I | B | |||||||||
| J | ||||||||||
| H | ||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
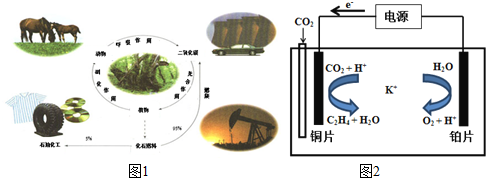
温度(℃) 气体总浓度 (mol/L) 时间(min) | 15 | 25 | 35 |
| 0 | 0 | 0 | 0 |
| t1 | 9×10-3 | 2.7×10-2 | 8.1×10-2 |
| t2 | 3×10-2 | 4.8×10-2 | 9.4×10-2 |
| t3 | 3×10-2 | 4.8×10-2 | 9.4×10-2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.4g金属镁变为镁离子时失去的电子数为0.1NA | |
| B. | 1molHCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等 | |
| C. | 6.4g铜与足量的硫磺在绝隔空气的条件下反应,电子转移的数目为0.1NA | |
| D. | 1mol白磷分子中所含共价键数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
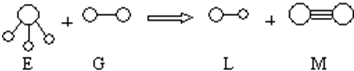
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com