
【题目】元素性质呈周期性变化的决定因素是______
A.元素原子半径大小呈周期性变化
B.元素的相对原子质量依次递增
C.元素原子核外电子排布呈周期性变化
D.元素的最高正化合价呈周期性变化
科目:高中化学 来源: 题型:
【题目】某分子的球棍模型如下图所示,图中“棍”代表单键或双键或三键;不同颜色的球代表不同元素的原子。有关该分子的说法错误的是:
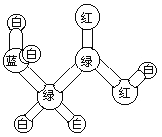
A. 不属于烃类 B. 能发生聚合反应
C. 不能与盐酸反应 D. 能与金属钠发生置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,pH=10的X、Y两种碱溶液各1mL,分别加水稀释到100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( ) 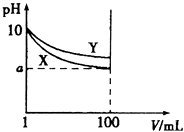
A.稀释前,两种碱溶液中溶质的物质的量浓度一定相等
B.稀释后,X溶液的碱性比Y溶液的碱性强
C.完全中和X、Y溶液时,消耗同浓度盐酸的体积VX>VY
D.若8<a<10,则X、Y都是弱碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表各组物质之间通过一步反应不可以实现如下图所示转化关系的是

选项 | X | Y | Z | 箭头上所标数字的反应条件 |
A | SiO2 | Na2SiO3 | H2SiO3 | ①与Na2CO3熔融 |
B | NaCl | NaHCO3 | Na2CO3 | ②加热 |
C | N2 | NO2 | HNO3 | ③加热 |
D | C | CO | CO2 | ④灼热炭粉 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列说法正确的是( )
A. 1 mol NaHCO3与足量盐酸反应放出CO2气体的体积为22.4L
B. 1 mol Al3+离子含有的核外电子数为3NA
C. O2和O3的混合气体,质量为48g,所含氧原子数为3NA
D. 高温下,0.2mol Fe与足量水蒸气反应,生成的H2的分子数目为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究PM 2.5、SO2、NOx等,对监测空气质量具有重要意义.取某样本用蒸馏水处理制成待测液,其中所含离子的化学组分及其浓度如下表:
离子 | K+ | Na+ | NH4+ | H+ | SO42﹣ | NO3﹣ | Cl﹣ |
浓度/molL﹣1 | 4×10﹣6 | 6×10﹣6 | 2×10﹣5 | a | 2×10﹣5 | 3×10﹣5 | 2×10﹣5 |
请回答下列问题:
(1)根据表中数据计算此待测液中c(H+)浓度a为________mol/L.
(2)NOx是汽车尾气中的主要污染物之一.
①汽车发动机工作时的高温会引发N2和O2反应,反应的化学方程式是__________.
②NOx能形成酸雨,由NO2形成酸雨的主要反应是______________(写化学方程式).
(3)为减少SO2的排放,常采取的措施有:
①在燃煤中加入生石灰可以起到固硫的作用,SO2被吸收后转化成一种硫元素的最高价态的化合物,该化合物常作为豆腐生产的原料,它在豆腐生产中的作用是___________.
②吸收烟气中的SO2,以下物质可作吸收剂的是_______(填序号);
a.NaOH b.H2SO4 c.NaHSO3 d. Na2SO3
硫酸工业中的尾气SO2可以循环利用,写出SO2转化为SO3反应的化学方程式_______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知难溶性物质K2SO4MgSO42CaSO4在水中存在如下平衡:K2SO4MgSO42CaSO4 (s)2Ca2++2K++Mg2++4SO42﹣ . 不同温度下,K+的浸出浓度与溶浸时间的关系如图所示,则下列说法错误的是( ) 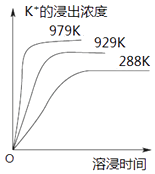
A.该平衡的Ksp=c2(Ca2+)c2(K+)c(Mg2+)c4(SO42﹣)
B.向该体系中加入饱和K2SO4溶液,溶解平衡向左移动
C.升高温度,溶浸速率增大,平衡向正反应方向移动
D.向该体系中加入饱和NaOH溶液,溶解平衡不发生移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M2O7x-与S2-在酸性溶液中发生如下反应:M2O7x-+3S2-+14H+2M3++3S↓+7H2O,则M2O7x-中M的化合价是( )
A. +2 B. +4 C. +6 D. +3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com