
| A、Mg | B、K | C、Br2 | D、I2 |
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
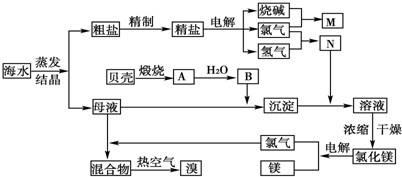
2- 4 |
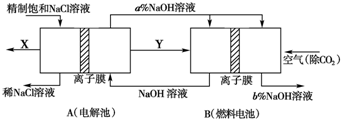
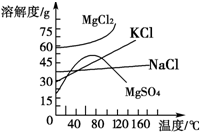
查看答案和解析>>
科目:高中化学 来源:2014届浙江省杭州市高一上学期期中七校联考化学试卷 题型:选择题
(12分)我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务。
(1)被称作海洋元素的是 ▲ (写元素符号)。
(2)工业上常以食盐为原料制备氯气,再用氯气制备漂白粉,请写出漂白粉长期露置在空气中失效的反应的化学方程式 ▲ 。
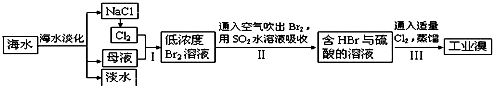
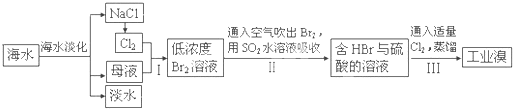
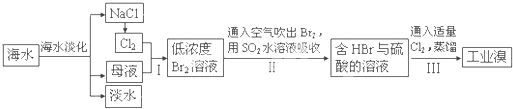
(3)从海水中提取食盐和溴的过程如下:
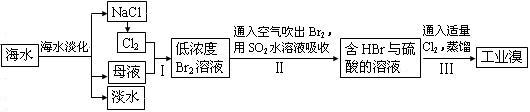
Ⅰ.①步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br¯,其目的为富集溴元素,请写出步骤Ⅱ的化学方程式, ▲ 。
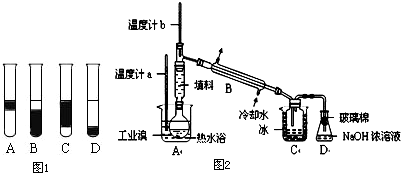
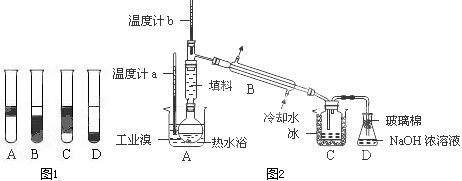
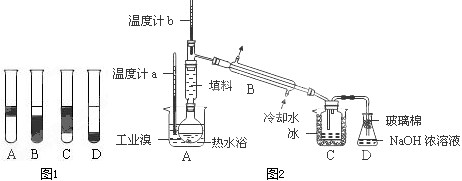
 ②在3mL溴水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象为右图中 ▲ 。
②在3mL溴水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象为右图中 ▲ 。
Ⅱ.某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如右装置简图:
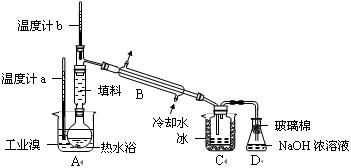
 请你参与分析讨论:
请你参与分析讨论:
①实验装置气密性良好,要在C中获得纯净的液溴即达到提纯溴的目的,操作中控制的关键条件是: ▲ 。
②为除去该产物中仍残留的少量Cl2,可向其中加入 ▲ 溶液,充分反应后,再进行的分离操作是 ▲ 。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com