
| A.不同的化学反应具有不同的反应热 |
| B.中和热△H=" -" 57.3kJ·mol-1,所以1.00L 1.00mol·L-1H2SO4与稀的NaOH溶液恰好完全反应放出57.3kJ的热量 |
| C.用等体积的0.50mol·L-1盐酸、0.55mol·L-1NaOH溶液进行中和热测定的实验,会使测得的值偏大 |
| D.在101KPa时,1molCH4完全燃烧生成CO2和水蒸气放出的热量就是CH4的燃烧热 |
科目:高中化学 来源:不详 题型:单选题
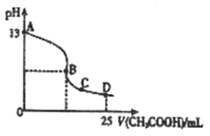
| A.a<7时,水的电离受到抑制 | B.a>7时,水的电离受到抑制 |
| C.a<7时,溶液的pH可能为a | D.a>7时,溶液的pH可能为14-a |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
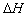 的绝对值均正确)( )
的绝对值均正确)( )A.C2H5OH(l)+3O2(g) = 2CO2 (g)+3H2O(g) kJ/mol(燃烧热) kJ/mol(燃烧热) |
B.NaOH(aq)+HCl (aq) = NaCl (aq) +H2O(l) kJ/mol(中和热) kJ/mol(中和热) |
C.S(s)+O2(g) = SO2(g) kJ/mol(反应热) kJ/mol(反应热) |
D.Fe+S = FeS kJ/mol(反应热) kJ/mol(反应热) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H="-483.6" kJ/mol
H="-483.6" kJ/mol H="-57.3" kJ/mol
H="-57.3" kJ/mol| A.H2的燃烧热为285.8 kJ/mol |
B.H2和O2反应生成液态水时的热化学方程式为H2(g) +1/2O2(g)=H2O(l) H="-571.6" kJ/mol H="-571.6" kJ/mol |
| C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ |
| D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH = 2的硫酸 | B.pH = 2的醋酸 | C.0.01 mol/L甲酸 | D.0.01 mol/L硝酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com