
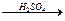 H2
H2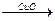 Cu
Cu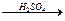 CuSO4
CuSO4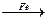 Cu
Cu| A.一样多 | B.①多 | C.②多 | D.无法判断 |
科目:高中化学 来源:不详 题型:单选题
| A.该反应中氧化剂与还原剂物质的量之比为1︰8 |
| B.若有lmol NO3— 发生还原反应,转移电子数为5mol |
| C.该反应说明Fe(NO3)2溶液不宜加酸酸化 |
| D.若把该反应设计成原电池,负极反应为Fe2+—e— =Fe 3+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.5.6 g | B.2.8 g | C.14 g | D.8.4 g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
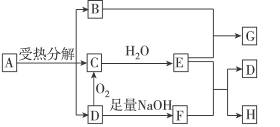
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入纯Cu将Fe2+还原 |
| B.向溶液中加入(NH4)2S使Fe2+沉淀 |
| C.直接加入水加热使杂质离子水解除去 |
| D.在溶液中通入Cl2,再加入CuO粉末调节pH为4~5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Fe(OH)2+2H+
Fe(OH)2+2H+| A.平衡向左移动,溶液浅绿色加深 |
| B.平衡向右移动 |
| C.溶液由浅绿色变成黄色 |
| D.无明显变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com