


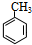
 ;已知C中含有9个碳原子,则A中含有2个碳原子,而且A是石油裂解气的主要成分之一,所以A为CH2=CH2;所以B为CHBrCHBr,即1,2-二溴乙烷;B与H反应生成C9H11Br,而且其苯环上的一卤代物只有两种,所以C的结构简式为
;已知C中含有9个碳原子,则A中含有2个碳原子,而且A是石油裂解气的主要成分之一,所以A为CH2=CH2;所以B为CHBrCHBr,即1,2-二溴乙烷;B与H反应生成C9H11Br,而且其苯环上的一卤代物只有两种,所以C的结构简式为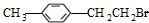 ;C反应生成D,D的分子式为C9H12O,则D为
;C反应生成D,D的分子式为C9H12O,则D为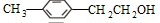 ;D发生氧化反应生成E,则E为
;D发生氧化反应生成E,则E为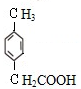 ;C一定条件下生成F,F反应生成G为高聚物,则F含有C=C,所以C生成F的反应为消去反应,所以F为
;C一定条件下生成F,F反应生成G为高聚物,则F含有C=C,所以C生成F的反应为消去反应,所以F为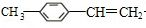 ,据此解答.
,据此解答. ;已知C中含有9个碳原子,则A中含有2个碳原子,而且A是石油裂解气的主要成分之一,所以A为CH2=CH2;所以B为CHBrCHBr,即1,2-二溴乙烷;B与H反应生成C9H11Br,而且其苯环上的一卤代物只有两种,所以C的结构简式为
;已知C中含有9个碳原子,则A中含有2个碳原子,而且A是石油裂解气的主要成分之一,所以A为CH2=CH2;所以B为CHBrCHBr,即1,2-二溴乙烷;B与H反应生成C9H11Br,而且其苯环上的一卤代物只有两种,所以C的结构简式为 ;C反应生成D,D的分子式为C9H12O,则D为
;C反应生成D,D的分子式为C9H12O,则D为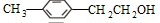 ;D发生氧化反应生成E,则E为
;D发生氧化反应生成E,则E为 ;C一定条件下生成F,F反应生成G为高聚物,则F含有C=C,所以C生成F的反应为消去反应,所以F为
;C一定条件下生成F,F反应生成G为高聚物,则F含有C=C,所以C生成F的反应为消去反应,所以F为 .
.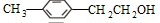 ,故答案为:
,故答案为: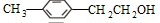 ;
; ,
, ;
;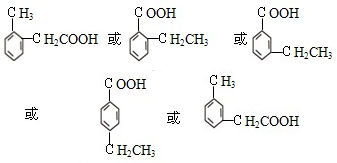 ,即含有5种同分异构体,
,即含有5种同分异构体, .
.


科目:高中化学 来源: 题型:
A、Fe2+、NH4+、Cl-、NO
| ||
| B、Na+、K+、Cl-、AlO2- | ||
| C、K+、Ba2+、Cl-、NO3- | ||
| D、Fe3+、Al3+、Cl-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ⑦ | ||||||
| 三 | ① | ③ | ⑤ | ⑧ | ||||
| 四 | ② | ④ | ⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 相对分子质量为174的有机物M中只含有C、H、O三种元素,其分子结构如图所示.
相对分子质量为174的有机物M中只含有C、H、O三种元素,其分子结构如图所示. ,试写出该反应的化学方程式
,试写出该反应的化学方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫化钠的水解反应:S2-+H3O+?HS-+H2O | ||||
B、用铜做阳极电解氯化铜溶液:Cu2++2Cl-
| ||||
| C、在硫酸亚铁溶液中通入氧气:4Fe2++O2+4H+=4Fe3++2H2O | ||||
| D、在氢氧化钡溶液中滴加硫酸氢钾溶液至pH=7:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②:
氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②:| A、工业上进行氨催化氧化生成 NO时,温度应控制在780~840℃之间 |
| B、工业上采用物料比n(O2)/n(NH3)在1.7~2.0,主要是为了提高反应速率 |
| C、在加压条件下生产能力可提高5~6倍,是因为加压可提高转化率 |
| D、氮气氧化为NO的热化学方程式为:N2(g)+O2(g)?2NO(g);△H=+181.5 kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com