
| 2 |
| 9 |
| 1mol |
| 4.5mol |
| 2 |
| 9 |
| 2 |
| 9 |
| 0.5mol |
| 1mol |
| 1mol |
| 4.5mol |
| 2 |
| 9 |
| 2 |
| 9 |
| 2 |
| 9 |
| 2 |
| 9 |


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
| A、①⑤⑦ | B、②③④⑥ |
| C、①④⑤ | D、⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4.48L | B、5.6L |
| C、6.72L | D、8.96L |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
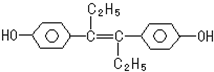
| A、1mol该有机物完全燃烧需要22 mol O2 |
| B、可与NaOH发生反应 |
| C、1mol该有机物可以与7mol Br2发生反应 |
| D、该有机物遇FeCl3溶液呈紫色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、煤中含有单质碳、苯、二甲苯、焦炉气 |
| B、煤的干馏是物理变化 |
| C、煤由复杂的有机物和无机物组成,煤的干馏是化学变化 |
| D、煤主要含有碳和氢两种元素,同时还含有少量的硫、氧、氮等元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
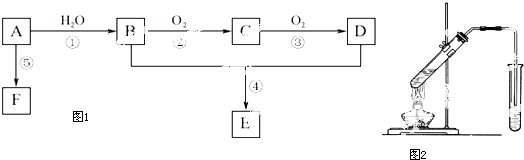
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C2H2、C2H6 |
| B、C2H4、C3H8 |
| C、C2H4O、C3H6O |
| D、CH2O、C6H12O6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该材料属于新型无机非金属材料 |
| B、该材料的化学性质非常稳定 |
| C、与金属一样有较好的传热性能 |
| D、可以替代金属做耐高温结构材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com