
����Ŀ�����������壨NiSO47H2O�������ڵ�ƹ�ҵ�����ú����ϴ���Ϊԭ�����Ʊ�����֪ij�������ĺ����ϴ�����Ҫ����Ni��������Al��Fe�ĵ��ʼ������������ʣ�����������ijС��ͨ���������ϣ����������ͼ��ʾ���Ʊ����̣�

��֪�� Ksp[Fe(OH)3]=4.0��10-38 ��Ksp[Ni(OH)2]=1.2��10-15
��1��������������з�����Ӧ�����ӷ���ʽ��_______________________________��
��2������a���õ��IJ����������ձ���________��________������c������Ϊ____________��____________�����ˡ�ϴ�ӡ�
��3���������______________����H2O2��Ŀ���ǣ������ӷ���ʽ��ʾ��_____________��
��4����pHΪ2-3ʱ���ӵ�����________��
��5������bΪ������Һ��pH������������b����Һ��c��Ni2����=2mol��L-1����������ǡ����ȫ������Һ��c��Fe3����=1.0��10-5mol��L-1ʱ����Һ���Ƿ���Ni(OH)2�������ɣ�________����ǡ�����
��6��NiSO47H2O�������Ʊ������أ�NiMH����������Ŀǰ�Ѿ���Ϊ��϶���������һ����Ҫ������ͣ�NiMH�е�M��ʾ���������Ͻ𣮸õ���ڷŵ�������ܷ�Ӧ�Ļ�ѧ����ʽ��NiOOH+MH=Ni(OH)2+M����NiMH��س������У������ĵ缫��ӦʽΪ_______��
���𰸡� 2Al+2OH-+2H2O�T2AlO2-+3H2�� ©�� ������ ����Ũ�� ��ȴ�ᾧ �������� 2Fe2++H2O2+2H+=2Fe3++2H2O ���ᣨH2SO4�� �� Ni(OH)2 + OH- - e- = NiOOH + H2O
����������1��������Ʒ��ֻ�н�������ǿ����Һ������Ӧ����ƫ�����κ����������ӷ���ʽΪ��2Al+2OH-+2H2O�T2AlO2-+3H2������ȷ�𰸣�2Al+2OH-+2H2O�T2AlO2-+3H2����
��2������aΪ�������õ������������ձ���©�� ��������������Һ�еõ����������壨NiSO47H2O��������Ҫ�Ƴɸ���ʱ������Һ��Ȼ��������Ũ������ȴ�ᾧ�����ˡ�ϴ������ȷ����©�� ��������������Ũ������ȴ�ᾧ��
��3�������������ᣬֻ�����ʲ�������ͼ���Թ�����Dz������ʣ���Һ�д������������ӣ�����H2O2��Ŀ�ľ��������������ӱ�Ϊ�����ӣ����ӷ���ʽΪ��2Fe2++H2O2+2H+=2Fe3++2H2O����ȷ�𰸣��������ʣ�2Fe2++H2O2+2H+=2Fe3++2H2O��
��4�����Ҫ�õ�NiSO47H2O��Ϊ�˲������������ӣ���ü����������Һ��pH����ȷ�𰸣����ᣨH2SO4����
��5������֪ Ksp[Fe(OH)3]=4.0��10-38 ��Ksp[Ni(OH)2]=1.2��10-15������Ksp[Fe(OH)3]=c(Fe3+)��c3(OH-)=1.0��10-5��c3(OH-)=4.0��10-38, c3(OH-)=4.0��10-33 mol��L-1, c(OH-)=1.6��10-11 mol��L-1, Ni(OH)2��Ũ����QC= c(Ni2+)��c2(OH-)=2����1.6��10-11��2=5.12��10-22< Ksp[Ni(OH)2]=1.2��10-15����Һ��û��Ni(OH)2�������ɣ���ȷ�𰸣���
��6���ŵ�Ϊԭ��أ����Ϊ���أ�������������������Ӧ��Ni(OH)2��NiԪ����+2������ΪNiOOH�е�+3�ۣ�����������Ӧ�������ĵ缫��ӦʽΪNi(OH)2 + OH- - e- = NiOOH + H2O����ȷ�𰸣�Ni(OH)2 + OH- - e- = NiOOH + H2O��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰ�ҹ��Ļ����������������Ϊȼú����,����ȼúΪ���ĵ�����������ɵĻ�����Ⱦ����Լ������ҵ��չ��һ����Ҫ����,���е�������(NOx)�Ǽ̷۳��Ͷ�������֮��ȼú��վ�����������ص㡣
(1)ȼú��������ķ����ܶ�,��ʯ��ʯ��ʯ�෨����ˮ���ȡ�����ʯ��ʯ-ʯ�෨�����ԭ����һ����SO2+Ca(OH)2![]() CaSO3+H2O,Ȼ���ٽ����������Ƴ�ʯ��,д���÷�Ӧ�Ļ�ѧ����ʽ: ��
CaSO3+H2O,Ȼ���ٽ����������Ƴ�ʯ��,д���÷�Ӧ�Ļ�ѧ����ʽ: ��
(2)ȼú���������ɲ��ð�(NH3)��Ϊ��ԭ����,�ڴ������������ڵ�������,��������(NOx)�뻹ԭ��������Ӧ,�������ĵ�����ˮ,д�����������백��Ӧ�Ļ�ѧ����ʽ: ��
(3)�ҹ��Ļ��������������жԿ����ж�����������Ũ��(��λ����Ŀ����������������������)��ֵ���±���ʾ:
Ũ����ֵ(mg��m-3) | ||
һ���� | ������ | ������ |
0.15 | 0.50 | 0.70 |
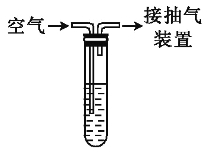
����ij��ѧ��ȤС�鰴ͼ��ʾ��ʵ��װ�ö�ij�ؿ����ж������������вⶨ:���Թ��м���1.00 mL 1.00��10-3 mol��L-1��ˮ,��������ˮ,�ټ���2~3�ε�����Һʹ��Һ����ɫ,ͨ������װ�û�������,ʹ�����ɵ����ܽ����Թ����ˮ��ַ�Ӧ,����Һ����ɫ��Ϊ��ɫʱ,ǡ����ȫ��Ӧ(��Ӧ�Ļ�ѧ����ʽ:SO2+I2+2H2O![]() H2SO4+2HI),ʵ������н����Թ��ڵĿ����������Ϊ0.1 m3�������˿����ж��������Ũ��Ϊ����mg��m-3,���ж϶��������Ũ�ȼ���Ϊ������
H2SO4+2HI),ʵ������н����Թ��ڵĿ����������Ϊ0.1 m3�������˿����ж��������Ũ��Ϊ����mg��m-3,���ж϶��������Ũ�ȼ���Ϊ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������X��һ��ҩ��ϳɵ��м��壬��ṹ��ʽ��ͼ��ʾ�������йػ�����X��˵����ȷ���ǣ� ��
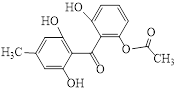
A. ������X�ķ���ʽΪC16H16O6
B. �ܷ����ӳɷ�Ӧ��ȡ����Ӧ����ȥ��Ӧ
C. 1mol������X������5molNaOH��7mol H2��4molBr2������Ӧ
D. ����FeCl3��Һ������ɫ��Ӧ�������ܷ���������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��N��P��As��Ga��Cr��Cu��Ԫ�ػ���������࣬������Ҫ���о���ֵ��Ӧ�ü�ֵ����ش��������⣺
��1��CrԪ�ؼ۵����Ų�ʽΪ__________________��
��2��N2F2�����У���ԭ�ӵ��ӻ��������Ϊ_______������N2F2���ܵĽṹʽ_____��
��3��PCl3��PCl5����Ԫ���γɵ�������Ҫ���������ݼ۵��ӻ��������Ʋ�PCl3�Ŀռ乹��__________________��
��4���黯���Ե������뵼�����ƣ��۵�Ϊ1230�棬���пռ���״�ṹ�����ܱȹ���������㷺�����״���Ӽ�������������ǡ�����ɴ��ȼ�˼����С�
���黯������____���塣��֪���������黯������ͬ�־������͡������־����۵�ϸߵ���___���ѧʽ������������____���������־����е�����Ԫ�ص縺����С����_____����Ԫ�ط��ţ���
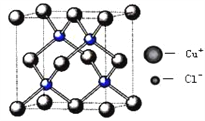
��5��ͭ�Ļ���������ܶ࣬��ͼ���Ȼ���ͭ�ľ����ṹ����֪�������ⳤΪa cm�����⻯��ͭ�ܶȵļ���ʽΪ��=_______g/cm3.(��NA��ʾ����ӵ�����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л������������������ܲ��ɷ֣������е�һЩ���ⳣ�漰��ѧ֪ʶ��
(1)�����м���ʳƷ��

�ٻ����������������������ҪӪ������Ϊ___________(����ࡱ������֬�������ʡ�)��
�ڳԷ�ʱ������һ�����о�����ζ������Ϊ���۷�����_____________(����ĸ)��Ӧ��
A.�ֽ� B.ˮ�� C.�ѽ�
(2)���ճ������У����������������________��
A.��ȼ�շ�����ë֯Ʒ����֯Ʒ
B.�ô���ϴ�ӹ����ϵ�����
C.������ζ�ķ�������ƺ��״�
D.�õ�����Һ����ӵ�ʳ�κͲ������ʳ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
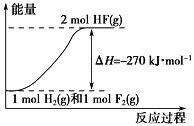
����Ŀ����֪��H2(g)��F2(g) ===2HF(g) ��H����270 kJ��mol��1������˵����ȷ����
A. ����ͬ�����£�1 mol H2(g)��1 mol F2(g)�������ܺ�С��2 mol HF(g)������
B. 1 mol H2(g)��1 mol F2(g)��Ӧ����2 molҺ̬HF�ų�����������270 kJ
C. �÷�Ӧ���淴Ӧ�Ƿ��ȷ�Ӧ
D. �÷�Ӧ���̵������仯������ͼ����ʾ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������д������( )
A.����Ũ���ᡢŨ���Ṳ�Ȳ�����50��60 �淴Ӧ����������
B.����ϩ(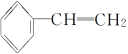 )�ں��������´�����������һ�������(
)�ں��������´�����������һ�������(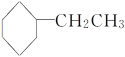 )
)
C.��ϩ��������Ȼ�̼��Һ��Ӧ����1,2��������
D.�ױ�(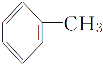 )�������ڹ��������·�Ӧ��Ҫ����2,4���ȼױ�(
)�������ڹ��������·�Ӧ��Ҫ����2,4���ȼױ�( )
)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A. ̫���ܵ�ؿ��ù������������Ӧ�������ڻ���������
B. SiO2������������ά
C. Na2SiO3ˮ��Һ�׳�ˮ������������ľ�ķ������𤽺��
D. ������Ͽ���ʹ���˴���ˮ�࣬ˮ�����л�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ��������,��һ�����ܱ�������,�ܱ�ʾ��ӦX(g)+2Y(g)![]() 2Z(g)һ���ﵽ��ѧƽ��״̬���� ( )
2Z(g)һ���ﵽ��ѧƽ��״̬���� ( )
��������������ܶȲ��ٷ����仯
��X��Y��Z��Ũ�Ȳ��ٷ����仯
�������е�ѹǿ���ٷ����仯
�ܵ�λʱ��������nmol Z,ͬʱ����2nmol Y
A.�٢� B.�ڢ� C.�ۢ� D.�٢�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com