
| A. | CO2,100 mL | B. | O2,200 mL | C. | N2,400 mL | D. | CH4,600 mL |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.
中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H<0表示放热反应,△H>0表示吸热反应 | |
| B. | 如果反应物所具有的总能量小于生成物所具有的总能量,则发生的反应是放热反应 | |
| C. | 在稀溶液中1mol酸和1mol碱完全反应所放出的热量,叫做中和热 | |
| D. | 1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4LCl2中含有NA个Cl2分子 | |
| B. | 1L 0.1mol.L-1Na2SO4溶液中有0.1NA个Na+ | |
| C. | 从1L1mol.L-1的NaCl溶液中取出10mL,其物质的量浓度为0.01mol.L-1 | |
| D. | 1molCa变成Ca2+时失去的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
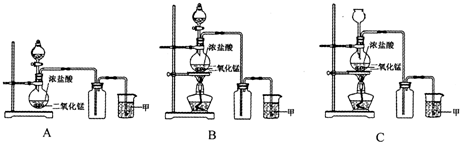
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH+HCl═NaCl+H2O | B. | MnO2+4HCl(浓)═MnCl2+2H2O+Cl2↑ | ||
| C. | Fe+2HCl═FeCl2+H2↑ | D. | CaCO3+2HCl═CaCl2+H2O+CO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com