
| A. | 增加C的量 | |
| B. | 将容器的体积缩小一半 | |
| C. | 保持体积不变,充入N2使体系压强增大 | |
| D. | 保持压强不变,充入N2使容器体积变大 |
分析 A.C为纯固体;
B.将容器的体积缩小一半,压强增大;
C.保持体积不变,充入N2,反应体系中各物质浓度不变;
D.保持压强不变,充入N2,体积增大,浓度减小.
解答 解:A.C为纯固体,增加C的量,反应速率不变,故A不选;
B.将容器的体积缩小一半,压强增大,反应速率增大,故B选;
C.保持体积不变,充入N2,反应体系中各物质浓度不变,反应速率不变,故C不选;
D.保持压强不变,充入N2,体积增大,浓度减小,反应速率减小,故D不选;
故选B.
点评 本题考查化学反应速率,为高频考点,把握浓度、压强对反应速率的影响为解答的关键,侧重分析与应用能力的考查,注意选项D为解答的易错点,题目难度不大.


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
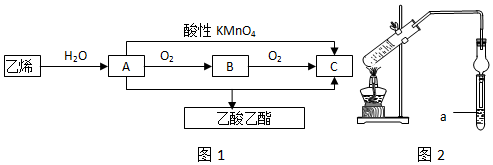
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 以石墨为电极电解MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$ Cl2+H2↑+2OH- | |
| B. | 泡沫灭火器工作时化学反应:2Al3++3CO32-+6H2O=Al(OH)3↓+3CO2↑ | |
| C. | KI溶液中滴入稀硫酸,空气中振荡:4H++4I-+O2═2I2+2H2O | |
| D. | 向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 它的二氯代物又有10种,立方烷
它的二氯代物又有10种,立方烷  它的六氯代物有3种.
它的六氯代物有3种. 分子中最多有25个原子共面.
分子中最多有25个原子共面.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/LCH3COOH溶液的pH>1:CH3COOH?CH3COO-+H+ | |
| B. | “NO2球”浸泡在冷水中,颜色变浅:2NO2(g)?N2O4(g)△H<0 | |
| C. | 向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H2O?Al(OH)3(胶体)+3H+ | |
| D. | 用催化法处理汽车尾气中的CO和NO:CO+NO$\frac{\underline{\;催化剂\;}}{\;}$C+NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,在下列各反应的类型中:①取代②加成③加聚④水解⑤酯化⑥中和⑦氧化⑧置换它能发生的反应有( )
,在下列各反应的类型中:①取代②加成③加聚④水解⑤酯化⑥中和⑦氧化⑧置换它能发生的反应有( )| A. | ①②③⑤⑥⑦ | B. | ②③①⑥⑧ | C. | ①②⑤⑥⑦⑧ | D. | ③④⑤⑥⑦⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com