
【题目】广泛用于纺织工业的连二亚硫酸钠(Na2S2O4),俗称保险粉,是一种强还原剂,可溶于水,但不溶于乙醇,在碱性介质中稳定。
Ⅰ.工业上制备连二亚硫酸钠的流程如下:

请回答下列问题:
(1)步骤①中的化学方程式为___________________________________;
(2)步骤②中沉淀为_________________________________(填化学式);
(3)步骤③中加入NaCl 固体的作用是______________________________,分离出保险粉方法为_______、洗涤、干燥,洗涤所用试剂是___________________________。
Ⅱ.工业上也可用右图装置电解NaHSO3溶液制Na2S2O4。
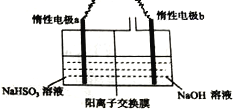
(1)惰性电极a连接电源的_________(填“正极”或“负极”),其电极反应式为________________;
(2)若不加隔膜,则得不到连二亚硫酸钠,其原因是____________________________。
Ⅲ.探究Na2S2O4的性质:
某课题小组常温下测定0.050 molL-1Na2S2O4溶液在空气中的pH变化如下图所示;
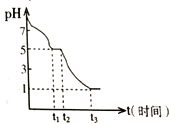
(1)0-t1段主要生成HSO3-,根据pH变化图,写出0- t1发生反应的离子方程式为______________;
(2)若t1时溶液中Na2S2O4全部被氧化成NaHSO3,此时溶液中c(SO32-)-c(H2SO3) =__________ molL-1(填具体数值,不考虑溶液体积变化)
【答案】 Zn+2SO2=ZnS2O4 Zn(OH)2 降低Na2S2O4的溶解度,使更多Na2S2O4析出 过滤 乙醇 负极 2HSO3-+2e-=S2O42-+2OH- Na2S2O4被阳极生成的氧气氧化或HSO3-在阳极失电子得到硫酸根 2H2O+2S2O42-+O2=4HSO3- 10-5-10-9
【解析】Ⅰ.锌粉加水形成分散系,再通入二氧化硫反应得到ZnS2O4,加入18%d NaOH溶液反应得到氢氧化锌沉淀、Na2S2O4,最后加入NaCl降低Na2S2O4的溶解度,析出Na2S2O4,溶液D中含有NaCl。
(1)根据上述分析,步骤①中的化学方程式为Zn+2SO2=ZnS2O4,故答案为:Zn+2SO2=ZnS2O4;
(2)步骤②中沉淀为Zn(OH)2,故答案为:Zn(OH)2;
(3)步骤③中加入NaCl 固体可以降低Na2S2O4的溶解度,使更多Na2S2O4析出,然后过滤、洗涤、干燥即可分离出保险粉;连二亚硫酸钠(Na2S2O4)是一种强还原剂,可溶于水,但不溶于乙醇。为了减少Na2S2O4的溶解损失,洗涤液可以选用乙醇,故答案为:降低Na2S2O4的溶解度,使更多Na2S2O4析出;过滤;乙醇;
Ⅱ. a极上NaHSO3生成Na2S2O4,S元素化合价由+4价降低到+3价,发生还原反应,应为阴极,a连接电源的负极,b极上氢氧化钠溶液中的水被氧化生成氧气,为阳极,b连接电源的正极。
(1)根据上述分析,惰性电极a连接电源的负极”),其电极反应式为2HSO3-+2e-=S2O42-+2OH-,故答案为:负极;2HSO3-+2e-=S2O42-+2OH-;
(2)若不加隔膜,Na2S2O4被阳极生成的氧气氧化得到硫酸根,得不到连二亚硫酸钠,故答案为:Na2S2O4被阳极生成的氧气氧化得到硫酸根;
Ⅲ.(1)Na2S2O4溶液在空气中易被氧化生成亚硫酸氢钠,则0~t1段发生离子反应方程式为 2S2O42-+O2+2H2O=4HSO3-,故答案为:2S2O42-+O2+2H2O=4HSO3-;
(2)若t1时溶液中Na2S2O4全部被氧化成NaHSO3,浓度为0.1 mol/L,根据图像,此时溶液的pH=5,溶液中存在物料守恒,c(SO32-)+c(H2SO3)+ c(HSO3-)=0.1 mol/L,也存在电荷守恒,c(Na+)+ c(H+)=2c(SO32-)+ c(HSO3-)+ c(OH-),则c(SO32-)-c(H2SO3)= c(Na+)+ c(H+)- c(OH-)-0.1 mol/L= c(H+)- c(OH-)=(10-5-10-9)mol/L,故答案为:10-5-10-9。


科目:高中化学 来源: 题型:
【题目】(1)①欲使蛋白质从水溶液中析出而又不改变它的主要性质,应加入________(填字母)。
a. 福尔马林 b. 饱和硫酸钠溶液 c. 硫酸铜溶液
②鉴别苯和甲苯的方法或试剂是________(填字母)。
a. 浓溴水 b. 酸化的KMnO4溶液 c. 在空气中点燃
③下列化合物中,常温常压呈液态的是________(填字母)。
a. 甲醇 b. 乙炔 c. 丙烯
(2)制备聚酯玻璃钢需要下列四种物质:

① 甲中不含氧原子的官能团是________(填名称)。
② 淀粉通过下列转化可以得到乙(其中A~D均为有机物):

A的化学式是________,C→D的反应类型是________。
③ 丙发生加聚反应的生成物为________________________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蒸馏是实验室制备蒸馏水的常用方法,如图所示的两个装置都可以制取蒸馏水。

(1)图Ⅰ是实验室制取蒸馏水的常用装置,仪器A、B、C的名称分别是_________、________、_______。加热A时要加垫石棉网,目的是_________________________________。
(2)图Ⅰ中冷凝水的流向是否正确?____(填“正确”或“不正确”),理由是_______________。
(3)实验时A中除加入少量自来水外,还需加入少量____,其作用是____________。
(4)图Ⅱ装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与图Ⅰ完全相同。该装置中使用的玻璃导管较长,其作用是_______________;烧杯中还应盛有的物质是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组的同学对一粗盐样品进行初步提纯。所用实验仪器或用品如下

(1)D的名称是__________。
(2)提纯的步骤是:溶解、过滤、__________。
(3)“过滤”操作的要点可概括为“一贴、二低、三靠”,其中的“二低”是__________、__________。
(4)该实验中多次利用仪器B__________(填名称)和仪器__________(填字母序号),且该仪器使用了__________次。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘是人体必需的微量元素,在医药和工业中都有广泛用途,因此从含碘废液中回收碘充分利用二次资源是非常重要的。实验室从含碘废液(除H2O外,含有CCl4、I2、I-)中回收碘,其实验过程如图1:(己知氧化性Cl2> IO3-)
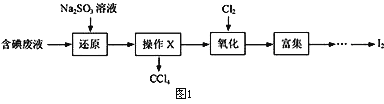
(1)向含碘废液中加入稍过量的Na2SO3溶液,反应的离子方程式为_________,该操作将I2还原为I-的目的是_________________________________________;
(2)操作X的名称为______________________________________;
(3)氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH约为2,通入Cl2,在40℃左右反应(实验装置如图2所示)。下列有关说法正确的是_____(填字母)。
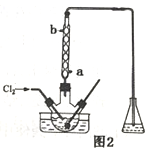
a.在实验中要缓慢通入氯气。提高氯气的利用率,防止产生污染
b.控制在较低温度下进行的主要原因是增大氯气的溶解度
c.通入过量的氯气可提高碘的产量
d.为有效防止碘的挥发水应从b口通入
e.锥形瓶中应盛放NaOH溶液
(4)二氧化氯(C1O2,黄绿色易溶于水的气体)是高效、低毒的消毒剂和水处理剂。现用C1O2氧化酸性含I-废液回收碘。
①写出C1O2氧化I-的离子方程式____________________________________。
②若处理含I-相同量的废液回收碘、所需Cl2的物质的量是C1O2的______________倍。
(5)已知:5SO32-+2IO3-+2H+![]() I2+5SO42-+H2O。某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO3-中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO3-的实验方案:(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)
I2+5SO42-+H2O。某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO3-中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO3-的实验方案:(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)
①取适量含碘废水用CCl4多次萃取、分液,直到水层检验不出碘单质存在;
②_______________________;
③另从水层取少量溶液,加入2-3滴淀粉溶液,滴加________________(填试剂和现象)。说明废水中含有IO3-,否则说明废水中不含IO3-。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向容积可变的密闭容器中通入N2和H2,发生反应:N2(g)+3H2(g) ![]() 2NH3(g)ΔH<0达到平衡后,试回答下列问题:
2NH3(g)ΔH<0达到平衡后,试回答下列问题:
(1)该条件下,反应的平衡常数表达式K=______;若降低温度,K值将______(填“增大”、“减小”或“不变”)。
(2)达到平衡后,若其它条件不变,把容器体积缩小一半,平衡将____(填“向逆反应方向”、“向正反应方向”或“不”)移动,平衡常数K将_____ (填“增大”、“减小”或“不变”)。
(3)达到平衡后,在恒压条件下,向容器中通人氦气(He),氮气的转化率将___(填“增大”、“减小”或“不变”)。
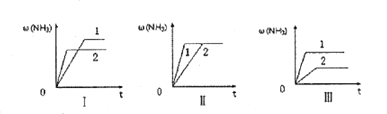
(4)在三个相同的容器中各充入1molN2和3molH2,在不同条件下分别达到平衡,氨的体积分数ω随时间变化如图所示。下列说法正确的是_______ (填序号)。
a.图I可能是不同压强对反应的影响,且P2>P1
b.图Ⅱ可能是同温同压下催化剂对反应的影响,且催化性能1>2
c.图Ⅱ可能是不同温度对反应的影响,且T1>T2
(5)A、B两个容积相同的容器中各充入1molN2和3molH2,A容器保持恒温恒容达到平衡时氢气的物质的量为x,B容器保持恒温恒压达到平衡时氢气的物质的量为y,则x____y(“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填写下列空白:
(1)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为____________。
(2)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为__________。
(3)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为__________,该混合气体对氢气的相对密度为________。
(4)已知a g A和b g B恰好完全反应生成0.2 mol C和d g D,则C的摩尔质量为__________________。
(5)同温同压下,已知O2的密度为ρg/L,则CO2的密度为__________。
(6)现有下列三种气体:①32 g CH4;②约含有6.02×1023个HCl分子的氯化氢气体;③标准状况下33.6 LO2。请按物理量由小到大的顺序排列:a.质量________(填序号,下同);b.分子数目________c.相同状况下气体的体积________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、恒容条件下,能使A(g)+B(g)C(g)+D(s) 正反应速率增大的措施是
A. 减小C或D的浓度 B. 再加入一定量D
C. 减小B的浓度 D. 增大A或B的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组实验中溶液最先变浑浊的是( )
A. 0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度10℃
B. 0.1mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度10℃
C. 0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度30℃
D. 0.2mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度30℃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com