
| A. | 为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 | |
| B. | 做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸.如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加 | |
| C. | 在未知溶液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液中存在SO42-或SO32- | |
| D. | 提纯混有少量硝酸钾的氯化钠,应采用在较低温度下制得浓溶液再冷却结晶、过滤、干燥的方法 |
分析 A、氯水中的次氯酸能漂白pH试纸;
B、液体加热要加沸石或碎瓷片,防止暴沸,如果加热一段时间后发现忘记加碎瓷片,应该采取停止加热,待溶液冷却后重新添加碎瓷片;
C、硫酸钡和AgCl均为不溶于酸的白色沉淀;
D、氯化钠中混有少量的硝酸钾,不能制得硝酸钾的饱和溶液.
解答 解:A、氯水中的次氯酸能漂白pH试纸,不能用pH试纸测定新制氯水的pH值,故A错误;
B、液体加热要加沸石或碎瓷片,引入汽化中心,可防止溶液暴沸,如果加热一段时间后发现忘记加碎瓷片,应该采取停止加热,待溶液冷却后重新添加碎瓷片,故B正确;
C、硫酸钡和AgCl均为不溶于酸的白色沉淀,则向某溶液中加入BaCl2溶液生成白色沉淀,继续加稀硝酸沉淀不消失,溶液中可能含Ag+,故C错误;
D、氯化钠中混有少量的硝酸钾,氯化钠是大量的,制得的饱和溶液中硝酸钾量较少,不能采取降温结晶的方法,故D错误,
故选B.
点评 本题主要考查的是实验室中常见操作和物质的提纯与检验,难度不大,注意D为易错点,若硝酸钾中混有少量的氯化钠,可以采用此方法提纯.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
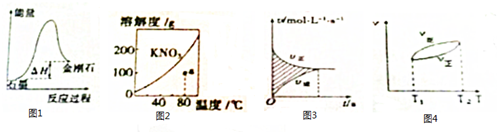
| A. | 由图1可知,从能量角度考虑,金刚石比石墨更稳定 | |
| B. | 图2中a点降温后加入KNO3 固体都能转变成饱和溶液 | |
| C. | 图3中阴影部分的面积表示△v=v正-v逆 | |
| D. | 由图4可知,正反应△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
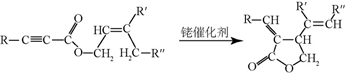

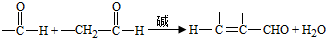
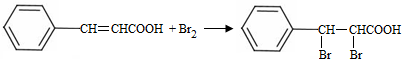 ;试剂b是NaOH、醇溶液.
;试剂b是NaOH、醇溶液.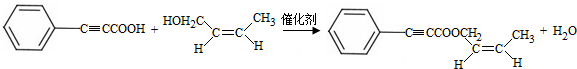 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,H2S浓度增加,表明该反应是吸热反应 | |
| B. | 通入CO后,正反应速率逐渐增大 | |
| C. | 反应前H2S物质的量为7mol | |
| D. | CO的平衡转化率为80% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
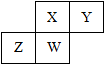 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )| A. | 原子半径:W>Z>Y>X | |
| B. | 最高价氧化物对应水化物的酸性:X>W>Z | |
| C. | 最简单气态氢化物的热稳定性:Y>X>W>Z | |
| D. | 元素X、Z、W的最高化合价分别与其主族序数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
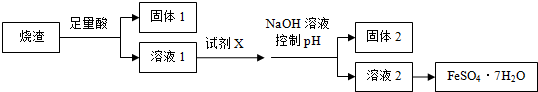
| A. | 溶解烧渣选用足量硫酸,试剂X选用铁粉 | |
| B. | 固体1中一定含有SiO2,控制pH是为了使Al3+转化为Al(OH)3,进入固体2 | |
| C. | 从溶液2得到FeSO4•7H2O产品的过程中,须控制条件防止其氧化和分解 | |
| D. | 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4•7H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3 | B. | Na2O | C. | FeCl2 | D. | SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2CN-+Cl2→(CN)2+2Cl- | B. | (CN)2+H2O→2H++CN-+CNO- | ||
| C. | (CN)2+2OH-→CN-+CNO-+H2O | D. | (SCN)2+2CN-→2SCN-+(CN)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com