
【题目】实验室有一未知浓度的NaOH溶液,某兴趣小组打算用已知浓度的稀硫酸来确定该NaOH溶液的浓度,现进行如下实验,请按要求完成题中填空。
步骤一:配制240mL 1.00mol/L的H2SO4标准溶液
相关操作:①计算;②量取;③稀释、冷却;④转移、洗涤;⑤定容;⑥摇匀。
(1)现用98%的浓硫酸(密度约为1.8g/cm3)来配制,需用量筒量取浓硫酸的体积为_____。
(2)实验中所用到的玻璃仪器有烧杯、玻璃棒、量筒、_____________、_______________。
(3)下列操作中会引起所配稀硫酸浓度偏大的操作有_______________。(填字母)
A.用量筒量取浓硫酸时,俯视读数
B.从量筒中倒出量取的浓硫酸后洗涤量筒内壁并把洗涤液转入容量瓶中
C.稀释浓硫酸时有少量液体溅出
D.浓硫酸稀释后未冷却就立即转移到容量瓶中
E.容量瓶中残留少量水即用来配溶液
F.定容摇匀后,发现液面低于刻度线
(4)简述上述配溶液时步骤⑤定容时的操作______________________________________。
步骤二:滴定
相关操作:取20.00mL待测NaOH溶液,向其中滴加步骤一配制的1.00mol/L H2SO4标准溶液,通过某种手段确定恰好完全反应时消耗H2SO4标准溶液15.00mL。
(5)通过实验确定该待测NaOH溶液的浓度为_____________(结果保留两位小数)。
(6)若因为操作不当造成步骤一配制的H2SO4标准溶液浓度偏大,但正常进行步骤二的操作,则导致测得的NaOH溶液的浓度比实际_______。(填“偏大”、“偏小”、“无影响”)
【答案】13.9mL 250mL容量瓶 胶头滴管 BD 将蒸馏水注入容量瓶,液面离容量瓶颈刻度线下1~2cm时,改用胶头滴管滴加蒸馏水至液面与刻度线相切 1.50mol/L 偏小
【解析】
(1)配制240mL 1.00mol/L的H2SO4,用250 mL的容量瓶,根据稀释前后硫酸的物质的量不变计算浓硫酸的体积;
(2)根据配制溶液的步骤分析实验中所用到的玻璃仪器;
(3)根据![]() 分析实验误差;
分析实验误差;
(4)根据定容操作回答;
(5)滴定终点时,酸碱恰好完全反应;
(6)H2SO4标准溶液浓度偏大,则消耗H2SO4标准溶液的体积偏小;
(1)98%的浓硫酸的物质的量浓度是![]() =18mol/L,稀释前后硫酸的物质的量不变,需用量筒量取浓硫酸的体积为
=18mol/L,稀释前后硫酸的物质的量不变,需用量筒量取浓硫酸的体积为![]() mL;
mL;
(2)实验需用250mL容量瓶定容,定容时用胶头滴管加水,所以用到的玻璃仪器有烧杯、玻璃棒、量筒、250mL容量瓶、胶头滴管;
(3)A.用量筒量取浓硫酸时,俯视读数,所取浓硫酸体积偏小,所配稀硫酸浓度偏小,故不选A;
B.从量筒中倒出量取的浓硫酸后洗涤量筒内壁并把洗涤液转入容量瓶中,硫酸物质的量偏大,所配稀硫酸浓度偏大,故选B;
C.稀释浓硫酸时有少量液体溅出,硫酸物质的量偏小,所配稀硫酸浓度偏小,故不选C;
D.浓硫酸稀释后未冷却就立即转移到容量瓶中,所配溶液体积偏小,所配稀硫酸浓度偏大,故选D;
E.容量瓶中残留少量水即用来配溶液,对所配稀硫酸浓度无影响,故不选E;
F.定容摇匀后,发现液面低于刻度线,对所配稀硫酸浓度无影响,故不选F;
(4)定容时的操作是:将蒸馏水注入容量瓶,液面离容量瓶颈刻度线下1~2cm时,改用胶头滴管滴加蒸馏水至液面与刻度线相切;
(5)滴定终点时,酸碱恰好完全反应,c(NaOH)×v(NaOH)= 2c(H2SO4)×v(H2SO4),c(NaOH)×0.02L= 2×1×0.015L;c(NaOH)= 1.50mol/L;
(6)H2SO4标准溶液浓度偏大,则消耗H2SO4标准溶液的体积偏小,测得的NaOH溶液的浓度比实际偏小。


科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是
A. 0.01mol L—1NH4Al(SO4)2溶液与0.02molL-1Ba(OH)2溶液等体积混合:NH4++Al3++2SO42— +2Ba2++4OH—=2BaSO4↓+Al(OH)3↓+NH3·H2O
B. 向甲醛溶液中加入足量的银氨溶液并加热:HCHO+2[Ag(NH3)2]++2OH—![]() HCOO-+NH4++2Ag↓+3NH3十H2O
HCOO-+NH4++2Ag↓+3NH3十H2O
C. 泡沫灭火器的灭火原理:2Al3++3CO32—+3H2O===2Al(OH)3↓+3CO2↑
D. 向苯酚钠溶液中通入少量CO2:2C6H5O—+CO2+H2O→2C6H5OH+CO32—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据图示填空

(1)化合物A中含氧官能团的名称是___________________________________。
(2)1mol A与2 mol H2反应生成1 mol E,其反应方程式是__________________________________。
(3)写出A发生加聚反应化学方程式____________________________。
(4)B在酸性条件下与Br2反应得到D,D的结构简式是_________________________。写出D与NaOH溶液反应的化学方程式_________________________________________。
(5)F的结构简式是______________。
(6)写出E发生缩聚反应的化学方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组模拟光合作用,采用电解CO2和H2O的方法制备CH3CH2OH和O2装置如图所示。下列说法不正确的是

A. 铂极为阳极,发生氧化反应
B. 电解过程中,H+由交换膜左侧向右侧迁移
C. 阴极的电极反应式为2CO2+12H++12e-====CH3CH2OH+3H2O
D. 电路上转移2mol电子时铂极产生11.2LO2(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同体积、相同pH的某一元强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是( )

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,用0.1000 mol/L的盐酸滴定25 mL 0.1000 mol/L Na2CO3溶液,所得滴定曲线如下图所示。下列有关滴定过程中溶液相关微粒浓度间的关系不正确的是
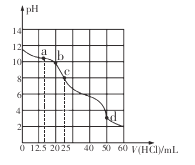
A. a点:c( HCO3-)>c(Cl-)>c(C032-)
B. b点:c(Na+)+c(H+)=c(Cl一)+c(HCO3-)+c(CO32-)+c(OH-)
C. c点:c(OH-)+c(CO32-)=c(H+)+c(H2CO3)
D. d点:c(Cl-)=c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K、Ka、KW分别表示化学平衡常数、电离常数和水的离子积常数,下列判断正确的是( )
A. 在500℃、20 MPa条件下,在5 L密闭容器中进行合成氨的反应,使用催化剂后K增大
B. 室温下Ka(HCN) < Ka(CH3COOH),说明CH3COOH电离产生的c(H+)一定比HCN电离产生的c(H+)大
C. 25℃时,pH均为4的盐酸和NH4I溶液中KW不相等
D. 2SO2+O2![]() 2SO3达平衡后,改变某一条件时K不变,SO2的转化率可能增大、减小或不变
2SO3达平衡后,改变某一条件时K不变,SO2的转化率可能增大、减小或不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组利用下列装置,进行与氯气相关的实验。
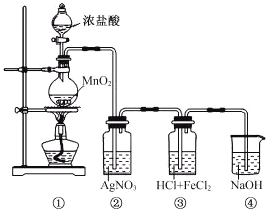
(1)装置④中NaOH溶液的作用是___________。
(2)实验结束后,取装置③中的溶液,经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到FeCl3·6H2O晶体。在蒸发浓缩操作中,不需要的仪器是___________。
A.蒸发皿 B.漏斗 C.玻璃棒 D.酒精灯
(3)装置②中出现白色沉淀,据此现象能否推测装置①中生成Cl2___________________,请说明理由_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】起固氮作用的化学反应的是
A. 工业上用氮气和氢气合成氨气B. 一氧化氮与氧气反应生成二氧化氮
C. 氨气经催化氧化生成一氧化氮D. 由氨气制碳酸氢铵和硫酸铵
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com