
| A. | 加催化剂,v正、v逆 都发生变化,且变化的倍数相等 | |
| B. | 加压,v正、v逆 都增大,且v正 增大的倍数大于V逆增大的倍数 | |
| C. | 增大氮气的浓度,N2的平衡转化率减小,H2的平衡转化率增大 | |
| D. | 降温,v正、v逆 都减小,且v正 减小的倍数大于v逆减小的倍数 |
分析 该反应是一个反应前后气体体积减小的、放热反应,根据温度、压强、催化剂对反应速率和化学平衡的影响来分析解答.
解答 解:A.催化剂能同等程度的改变正逆反应速率,故A正确;
B.增大压强,正逆反应速率都增大,但v正增大的倍数大于v逆增大的倍数,则平衡向正反应方向移动,故B正确;
C.增加一种反应物的浓度本身转化率减小,另一种物质的转化率变大,所以增大氮气的浓度,N2的平衡转化率减小,H2的平衡转化率增大,故C正确;
D.降低温度,正逆反应速率都减小,但正反应速率减小的倍数小于v逆减小的倍数,则平衡向正反应方向移动,故D错误;
故选D.
点评 本题考查了外界条件对化学反应速率和化学平衡的影响,易错选项是C,增加一种反应物的浓度本身转化率减小,另一种物质的转化率变大,为易错点.


科目:高中化学 来源: 题型:解答题
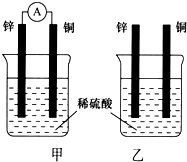 分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,甲中A为电流表.请回答下列问题:
分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,甲中A为电流表.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
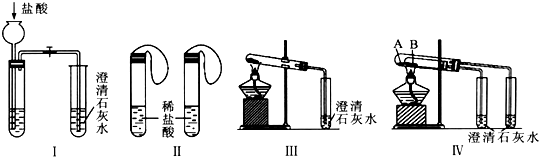
| 实验方案 | 预测现象 | 预测依据 |
| 操作1:向2 mL Na2CO3溶液中滴加1 mL 0.5 mol•L-1 CaCl2溶液 | 有白色沉淀 | Na2CO3溶液中的CO32-浓度较大,能与CaCl2发生反应Ca2++CO32-=CaCO3↓(写离子方程式) |
| 操作2:向2 mL NaHCO3溶液中滴加1 mL 0.5 mol•L-1 CaCl2溶液 | 无白色沉淀 | NaHCO3溶液中的CO32-浓度很小,不能与CaCl2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{a}{b}$ | B. | $\frac{a}{2b}$ | C. | $\frac{a}{a+2b}$ | D. | $\frac{b}{a}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 苯氧乙酸甲酯的分子式为C9H10O3 | |
| B. | 苯氧乙酸与邻羟基苯乙酸不互为同分异构体 | |
| C. | 苯酚和邻羟基苯乙酸可用FeCl3溶液检验 | |
| D. | ClCH2COOH与足量烧碱溶液共热所得有机物为HOCH2COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
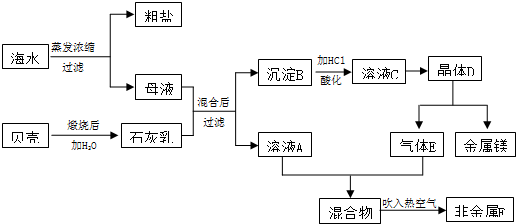
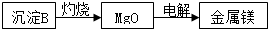
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 每摩尔花生四烯酸最多可与4 mol溴发生加成反应 | |
| B. | 它可以使酸性高锰酸钾溶液褪色 | |
| C. | 它可与乙醇发生酯化反应 | |
| D. | 它是食醋的主要成分 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com