
| A. | NH4Cl | B. | NH4HSO4 | C. | CH3COONH4 | D. | (NH4)2Fe(SO4)2 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 相同温度下,AgCl的溶解性比Ag2CO3强 | |
| B. | 沉淀转化反应2AgCl(s)+CO32-(aq)?Ag2CO3(s)+2Cl-(aq)的平衡常数为20mol•L-1 | |
| C. | 混合后溶液中的:c(Na+)>c (Cl-)>c (CO32-)>c (OH-)>c(H+) | |
| D. | 混合后溶液中的:c(Na+)+c(H+)+c(Ag+)=2 c(CO32-)+c(HCO3-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分别与同浓度的稀盐酸反应 | B. | 分别加入NaOH溶液 | ||
| C. | 分别加入石灰水 | D. | 溶于水,比较其溶解性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 充电时,Ni(OH)2为阳极 | |
| B. | 放电时,Fe为正极,Ni2O3为负极 | |
| C. | 该新型蓄电池的电解质溶液呈碱性 | |
| D. | 充电时,阴极反应式为Fe(OH)2+2e-=Fe+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
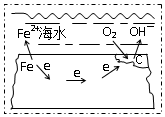
| A. | 电子从碳转移给铁 | |
| B. | 在钢铁上连接铅块,可起到防护作用 | |
| C. | 正极反应为:O2+2H2O+4e→4OH- | |
| D. | 该金属腐蚀过程为析氢腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
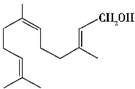
| A. | 金合欢醇与乙醇是同系物 | |
| B. | 金合欢醇可发生加成反应,但不能发生取代反应 | |
| C. | 1 mol 金合欢醇能与3 mol H2 反应,也能与3 mol Br2反应 | |
| D. | 1 mol 金合欢醇与足量Na 反应生成1mol 氢气,完全燃烧时消耗O2 21 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -183 kJ•mol-1 | B. | +183 kJ•mol-1 | C. | -862 kJ•mol-1 | D. | +862 kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com