
| A. | 短周期是指第1、2周期 | B. | 过渡元素全部是金属元素 | ||
| C. | 元素周期表有8个副族 | D. | IA族的元索全部是金属元素 |
分析 A.元素周期表的前3周期为短周期;
B.过渡元素包括7个副族和1个ⅤⅢ族,都是金属元素;
C.元素周期表中含有ⅠB~ⅤⅡB 7个副族;
D.ⅠA族元素中,H为非金属元素.
解答 解:A.周期表中,短周期为1、2、3周期,故A错误;
B.副族和ⅤⅢ族元素为过渡元素,都是金属元素,故B正确;
C.元素周期表中含有7个主族、7个副族、1个0族和1个ⅤⅢ族,故C错误;
D.H元素为ⅠA族元素,H元素为非金属元素,故D错误;
故选B.
点评 本题考查了元素周期表结构及其应用,题目难度不大,明确元素周期表结构为解答关键,注意掌握原子结构与元素周期表的关系,试题侧重基础知识的考查,培养了学生的灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅的分子式:SiO2 | |
| B. | 质子数为53,中子数为78的碘原子:${\;}_{53}^{131}$I | |
| C. | 甲基的电子式: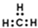 | |
| D. | 邻羟基苯甲酸的结构简式: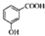 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
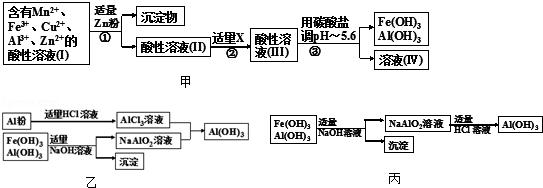
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
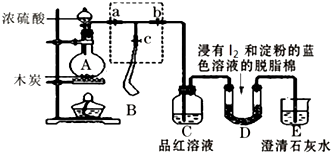
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
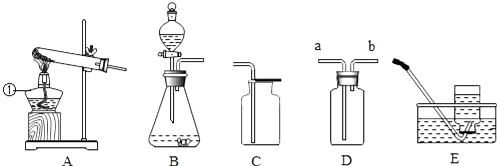
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
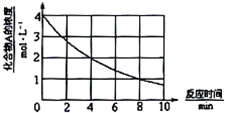 化合物A在一定条件下发生分解反应,反应物浓度随反应时间的变化如图所示.则化合物A在4~8min间的平均反应速率为( )
化合物A在一定条件下发生分解反应,反应物浓度随反应时间的变化如图所示.则化合物A在4~8min间的平均反应速率为( )| A. | 0.20 mol•L-1•min-1 | B. | 0.25 mol•L-1•min-1 | ||
| C. | 0.30 mol•L-1•min-1 | D. | 0.50 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 4 | 1 | 42 | 10 |
| 反应后质量/g | 待测 | 20 | 6 | 31 |
| A. | 该变化的基本反应类型是分解反应 | |
| B. | 参加反应的甲、丙的质量比为1:9 | |
| C. | 乙、丁的相对分子质量比一定为10:9 | |
| D. | 甲反应后的质量为8g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com