
 =2Cr(OH)3↓+3O2↑+2H2O,
=2Cr(OH)3↓+3O2↑+2H2O, =2Cr(OH)3↓+3O2↑+2H2O;H2CrO4;O2.
=2Cr(OH)3↓+3O2↑+2H2O;H2CrO4;O2.


科目:高中化学 来源: 题型:
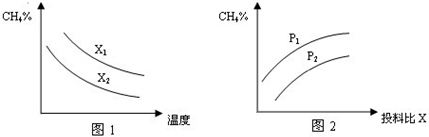
| c(H2)?c(CO) |
| c(H2O) |
| n(CH4) |
| n(H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 电解原理在化学工业中有广泛应用. 铝和氢氧化钠都是重要的工业产品.请回答:
电解原理在化学工业中有广泛应用. 铝和氢氧化钠都是重要的工业产品.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲烷的球棍模型需要用五个保龄球和五根竹签制作 |
| B、甲烷球棍模型中,较大的保龄球代表甲烷分子中的氢原子 |
| C、甲烷的球棍模型中,五个保龄球的球心不在同一平面上,其连线构成正四面体 |
| D、制作乙烷的模型时,需要用到七根完全相同的竹签 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com